16. 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
探究一:甲组同学设计了如图所示的实验,根据图示回答:
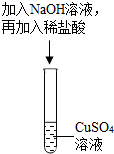
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
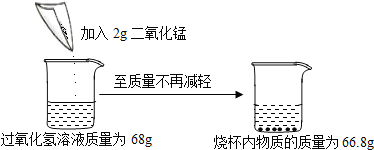
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
【得出结论】通过探究,同学们一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
0 147470 147478 147484 147488 147494 147496 147500 147506 147508 147514 147520 147524 147526 147530 147536 147538 147544 147548 147550 147554 147556 147560 147562 147564 147565 147566 147568 147569 147570 147572 147574 147578 147580 147584 147586 147590 147596 147598 147604 147608 147610 147614 147620 147626 147628 147634 147638 147640 147646 147650 147656 147664 211419
 某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.
某化学课堂围绕“酸和碱的中和反应”,将学生分成若干小组开展探究活动.请你参与学习并填写空格.探究一:甲组同学设计了如图所示的实验,根据图示回答:
(1)在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到的实验现象是产生蓝色沉淀.
(2)然后再向试管中加入稀盐酸,该实验通过稀盐酸与氢氧化铜(填物质名称)反应,观察到明显现象,验证了酸与碱能发生中和反应.
探究二:乙组同学将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中,一会儿后,发现忘记了滴加指示剂.于是他们从烧杯中取出少量反应后的溶液于试管中,滴入几滴酚酞溶液,振荡,观察到无明显现象.中和反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质组成是什么?
【假设猜想】针对疑问,大家纷纷提出猜想
猜想一:只有Na2SO4
猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH
同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的是猜想三.
【实验探究】为了验证其余猜想,同学们利用烧杯中的溶液,进行如下方案的探究.
| 实验方案 | 实验现象 | 结论与解释 |
方案一:滴加Na2CO3溶液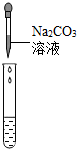 | 产生大量气泡 | 溶液中有H2SO4 |
方案二:滴加BaCl2溶液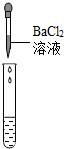 | 产生白色沉淀 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究给予了肯定,同时指出实验方案中有一个是错误的,错误的原因是方案二只能证明溶液中含有SO42-,不能证明含有H2SO4.
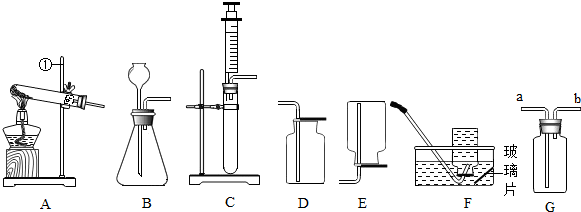
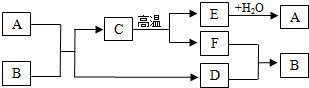 已知A、B、C、D、E、F六种物质之间存在如图所示的关系.其中A常用来改良酸性土壤,B是常见的盐,其水溶液显碱性,C是大理石的主要成分.(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题:
已知A、B、C、D、E、F六种物质之间存在如图所示的关系.其中A常用来改良酸性土壤,B是常见的盐,其水溶液显碱性,C是大理石的主要成分.(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题: