题目内容
4.苯(化学式:C6H6)是一种重要的有机溶剂,它的部分同系列物质如下:| 碳原子数 | 6 | 7 | 8 | 9 | 10 |
| 化学式 | C6H6 | C7H8 | X | C9H12 | C10H14 |
(2)在C6H6中,C与H元素质量比为12:1;
(3)156g C6H6 中含碳元素多少g?(要求写出计算过程)
分析 (1)根据苯的部分同系列物质的化学式,归纳分子构成中C、H原子个数的变化规律,根据规律判断物质X的分子含有8个C原子时H原子的个数,写出物质X的化学式;
(2)根据苯的化学式C6H6,根据组成元素质量比、组成元素的质量分数的计算公式计算C、H质量比;
(3)根据碳元素的质量分数和苯的质量进行计算.
解答 解:(1)由表中苯的部分同系列物质的化学式,C原子个数分别为6、7、8、9、10时,H原子的个数为6、8、X、12、14,可发现C原子增加一个时H原子增加两个,因此可得物质X的分子中H原子个数为10,则物质X的化学式为C8H10;
(2)C6H6中,C与H的质量比=(12×6):(1×6)=12:1;
(3)156g C6H6 中含碳元素质量为:156g×$\frac{72}{78}$=144g.
故答案为:(1)C8H10;
(2)12:1;
(3)144g.
点评 根据化合物的化学式,组成元素质量比为组成元素的相对原子质量与原子个数乘积的比,组成元素质量分数=$\frac{元素的相对原子质量×原子个数}{相对分子质量}$×100%.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.逻辑推理是化学学习和研究中常用的思维方法,下列推理正确的是( )
| A. | 水能灭火,所以电脑一旦失火应立即用水烧灭 | |
| B. | 碱溶液能使无色酚酞溶液变红,所以可以使无色酚酞溶液变红的一定是碱 | |
| C. | 稀硫酸滴入石蕊溶液变红色,所以盐酸滴入石蕊试液也变红色 | |
| D. | 氧化物都含有氧元素,所以含有氧元素的化合物都是氧化物 |
19.用符号表示:2个镁离子2Mg2+,4个铁原子4Fe,3个水分子3H2O,2个氢分子2H2,三氧化硫中硫元素显+6价$\stackrel{+6}{S}$O3,氧化铁Fe2O3,氯化亚铁FeCl2.
16.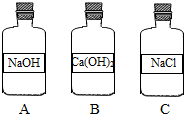 同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
(1)三个瓶中的白色固体一定是纯净物的是NaCl(填化学式).
(2)只用水不能清洗干净的细口瓶是B(填“A”或“B”或“C”).
(3)探究B瓶中白色固体的成分.
【提出问题】B中白色固体是什么物质?
【猜想与假设】
猜想1:可能是CaCO3 猜想2:可能是Ca(OH)2 猜想3:可能是 CaCO3和Ca(OH)2的混合物.
【设计实验】
①甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水也可能不溶解而沉淀.
②为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
(4)最后用稀盐酸和水将三个细口瓶洗净,洗后液体倒入一个干净的容器中,得到澄清无色溶液,写出其中一定含有的溶质NaCl、CaCl2.
 同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.(1)三个瓶中的白色固体一定是纯净物的是NaCl(填化学式).
(2)只用水不能清洗干净的细口瓶是B(填“A”或“B”或“C”).
(3)探究B瓶中白色固体的成分.
【提出问题】B中白色固体是什么物质?
【猜想与假设】
猜想1:可能是CaCO3 猜想2:可能是Ca(OH)2 猜想3:可能是 CaCO3和Ca(OH)2的混合物.
【设计实验】
①甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水也可能不溶解而沉淀.
| OHˉ | Clˉ | CO32ˉ | NO3ˉ | |
| Ca2+ | 微溶 | 溶 | 不 | 溶 |
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1-2滴无色酚酞试液 | ||
| 往上述试管中的残留的固体中加入稀盐酸 | 白色粉末中有(填“有”或“无”)CaCO3 |
13. 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,在右边的坐标纸上绘制出所加稀盐酸质量与生成气体质量关系的曲线.(不要求写出计算过程,只画出曲线即可)
14.某同学描述的有关实验现象如下,你认为正确的是( )
| A. | 硫在氧气中燃烧产生微弱的淡蓝色火焰,并生成有刺激性气味的气体 | |
| B. | 点燃棉制品时时产生烧焦羽毛的气味 | |
| C. | 将CO通入到灼热的氧化铜中,发现红色粉末立即变成黑色 | |
| D. | 将澄清的饱和石灰水加热,发现有白色浑浊出现 |