题目内容
16.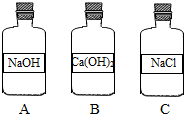 同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.
同学们在清理实验室时,发现如图三个内壁都有白色固体的细口瓶,请你和同学们一起完成清洗和以下探究活动.(1)三个瓶中的白色固体一定是纯净物的是NaCl(填化学式).
(2)只用水不能清洗干净的细口瓶是B(填“A”或“B”或“C”).
(3)探究B瓶中白色固体的成分.
【提出问题】B中白色固体是什么物质?
【猜想与假设】
猜想1:可能是CaCO3 猜想2:可能是Ca(OH)2 猜想3:可能是 CaCO3和Ca(OH)2的混合物.
【设计实验】
①甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解.于是他得出粉末中一定有CaCO3的结论.乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是:Ca(OH)2微溶于水也可能不溶解而沉淀.
| OHˉ | Clˉ | CO32ˉ | NO3ˉ | |
| Ca2+ | 微溶 | 溶 | 不 | 溶 |
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1-2滴无色酚酞试液 | ||
| 往上述试管中的残留的固体中加入稀盐酸 | 白色粉末中有(填“有”或“无”)CaCO3 |
分析 (1)根据纯净物的概念进行分析;
(2)考虑碳酸钙不溶于水,不溶于水的白色固体不能用水清洗干净;
(3)根据各物质的化学性质进行分析,考虑氢氧化钙易和二氧化碳生成碳酸钙和水.
【设计实验】
①考虑Ca(OH)2微溶于水也可能不溶解而沉淀.
②考虑氢氧化钙能使无色酚酞试液变红的性质;考虑碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;
(4)因为得到澄清无色溶液,考虑碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;推测其中一定含有的溶质.
解答 解:(1)氢氧化钠易和二氧化碳反应生成碳酸钠和水;氢氧化钙易和二氧化碳生成碳酸钙和水;氯化钠化学性质稳定,因此三个瓶中的白色固体一定是纯净物的是氯化钠.
(2)氢氧化钠、碳酸钠、氯化钠易溶于水,可用水洗去,碳酸钙不溶于水,因此只用水不能清洗干净的细口瓶是B氢氧化钙.
【设计实验】
①因为Ca(OH)2微溶于水也可能不溶解而沉淀,所以甲同学的结论(粉末中一定有CaCO3)不严密.
②
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1-2滴无色酚酞试液 | 无明显的现象 | 白色粉末中没有Ca(OH)2 |
| 往上述试管中的残留的固体中加入稀盐酸 | 有气泡生成 | 白色粉末中有CaCO3 |
故答案为:
(1)NaCl;(2)B;(3)【设计实验】①Ca(OH)2微溶于水也可能不溶解而沉淀;②无明显的现象;白色粉末中没有Ca(OH)2;有气泡生成;有;(合理即可)(4)NaCl、CaCl2;
点评 此题难度较大,掌握纯净物的概念,物质的溶解性以及酸碱盐的化学性质等是解题的关键.

练习册系列答案
相关题目
7.用分子的观点解释下列现象或事实,不合理的是( )
| A. | 水分蒸发--分子大小发生改变 | |
| B. | 热胀冷缩--分子间间隔改变 | |
| C. | 闻到花香--分子在不断地运动 | |
| D. | 过氧化氢分解--分子本身发生了变化 |
4.苯(化学式:C6H6)是一种重要的有机溶剂,它的部分同系列物质如下:
(1)比较归纳是学好化学的重要方法,据表推断X的化学式为C8H10;
(2)在C6H6中,C与H元素质量比为12:1;
(3)156g C6H6 中含碳元素多少g?(要求写出计算过程)
| 碳原子数 | 6 | 7 | 8 | 9 | 10 |
| 化学式 | C6H6 | C7H8 | X | C9H12 | C10H14 |
(2)在C6H6中,C与H元素质量比为12:1;
(3)156g C6H6 中含碳元素多少g?(要求写出计算过程)
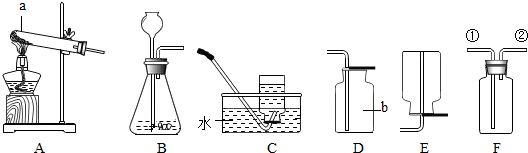
11.如图所示实验操作错误的是( )
| A. | 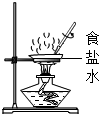 蒸发结晶 蒸发结晶 | B. | 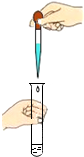 滴加液体 | ||
| C. |  熄灭酒精灯 熄灭酒精灯 | D. | 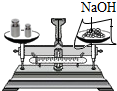 称量6.0克氢氧化钠 |
1.合理搭配饮食是我们的健康理念.中考备考期间,学校食堂午餐菜单是:米饭、红烧鲤鱼、炸鸡腿、牛大骨汤.这份午餐搭配中还缺少的营养素是( )
| A. | 维生素 | B. | 蛋白质 | C. | 油脂 | D. | 糖类 |
6.有关酸和碱的说法不正确的是( )
| A. | 不是所有的酸和碱都能发生中和反应 | |
| B. | 酸在水中解离出来的阳离子全部是H+ | |
| C. | 酸碱中和反应的实质是H+与OH-结合生成水 | |
| D. | 碱有共同的化学性质是因为有OH- |
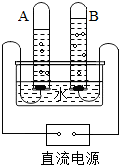 如图是水通电的简易实验装置,通电一会儿后,看到的现象是两电极上产生气泡;A试管中产生的气体是氢气;检验B试管内气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气;装置内发生反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;该实验得出的结论为水是由氢元素和氧元素组成的.
如图是水通电的简易实验装置,通电一会儿后,看到的现象是两电极上产生气泡;A试管中产生的气体是氢气;检验B试管内气体的方法是将带火星的木条伸入试管中,复燃则证明是氧气;装置内发生反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;该实验得出的结论为水是由氢元素和氧元素组成的.