题目内容
19. 为了验证二氧化碳的性质,某同学将实验中制取的二氧化碳气体导入A、B装置(如图),回答下列问题:
为了验证二氧化碳的性质,某同学将实验中制取的二氧化碳气体导入A、B装置(如图),回答下列问题:(1)装置A中的现象是溶液由紫色变为红色,发生反应的化学方程式为CO2+H2O=H2CO3;
(2)B装置中的现象是下面的蜡烛先熄灭上面的蜡烛后熄灭,说明二氧化碳不能燃烧,也不支持蜡烛燃烧,且密度比空气大,由此可知,二氧化碳在生活中可用于灭火.
分析 (1)根据二氧化碳能与水反应生成碳酸,碳酸能使紫色变红色分析解答;
(2)根据二氧化碳既不燃烧也不支持燃烧且密度比空气密度大分析解答;
解答 解:(1)将二氧化碳通入A装置连接,观察到的现象是溶液由紫色变为红色,因为二氧化碳能与水反应生成碳酸,碳酸能使紫色变红色,故答案为:溶液由紫色变为红色;CO2+H2O=H2CO3;
(2)二氧化碳既不燃烧也不支持燃烧且密度比空气密度大,所以下面的蜡烛先熄灭上面的蜡烛后熄灭,二氧化碳可以灭火;故答案:下面的蜡烛先熄灭上面的蜡烛后熄灭;灭火.
点评 本考点主要考查气体了二氧化碳的性质,同时也考查了化学方程式的书写和金属的性质,本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
9.(1)阅读下面短文并回答问题:
镁条是银白色固体,具有可燃性,在空气中点燃镁条,发出耀眼的白光,放出热量,生成一种白色的氧化镁粉末,镁的密度为1.7g/cm3,熔点为648.8℃,镁能与稀盐酸反应生成氢气.
上述叙述中:属于镁的物理性质有:银白色固体,密度为1.7g/cm3,熔点为648.8℃;
属于镁的化学性质有:具有可燃性,能与稀盐酸反应生成氢气;
可判断镁条燃烧发生化学变化的现象有:生成一种白色的氧化镁粉末.
(2)1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值.铟元素的核电荷数为49,相对原子质量为115.铟原子的核外电子数为49,核内质子数为49,核内中子数为66
(3)如表是元素周期表的一部分,请根据表中信息回答下列问題:
(1)氯元素的相对原子质量是35.45,在化学反应中容易得到(填“得到”或“失去”)电子.
(2)由原子序数为8和13的元素形成的化合物的化学式是Al2O3.
(3)第二、三周期的元素排列从左至右所遵循的规律是最外层电子数由1个依次增加到8个(写一种).
镁条是银白色固体,具有可燃性,在空气中点燃镁条,发出耀眼的白光,放出热量,生成一种白色的氧化镁粉末,镁的密度为1.7g/cm3,熔点为648.8℃,镁能与稀盐酸反应生成氢气.
上述叙述中:属于镁的物理性质有:银白色固体,密度为1.7g/cm3,熔点为648.8℃;
属于镁的化学性质有:具有可燃性,能与稀盐酸反应生成氢气;
可判断镁条燃烧发生化学变化的现象有:生成一种白色的氧化镁粉末.
(2)1991年,我国著名化学家张青莲教授与另一位科学家合作,测定了铟(In)元素的相对原子质量新值.铟元素的核电荷数为49,相对原子质量为115.铟原子的核外电子数为49,核内质子数为49,核内中子数为66
(3)如表是元素周期表的一部分,请根据表中信息回答下列问題:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | 1 H 氢 1.008 | 2 He 氦 4.003 | ||||||
| 二 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 20.18 |
| 三 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)由原子序数为8和13的元素形成的化合物的化学式是Al2O3.
(3)第二、三周期的元素排列从左至右所遵循的规律是最外层电子数由1个依次增加到8个(写一种).
4. 在我省金寨县境内发现世界第二大钼矿,其钼储量约有220万吨以上.在元素周期表中钼元素的相关信息如图所示,下列说法正确的是( )
在我省金寨县境内发现世界第二大钼矿,其钼储量约有220万吨以上.在元素周期表中钼元素的相关信息如图所示,下列说法正确的是( )
 在我省金寨县境内发现世界第二大钼矿,其钼储量约有220万吨以上.在元素周期表中钼元素的相关信息如图所示,下列说法正确的是( )
在我省金寨县境内发现世界第二大钼矿,其钼储量约有220万吨以上.在元素周期表中钼元素的相关信息如图所示,下列说法正确的是( )| A. | 元素符号为MO | B. | 属于非金属元素 | ||
| C. | 原子核内质子数为42 | D. | 相对原子质量为95.96g |
11.下列生产、生活中的变化,属于化学变化的是( )
| A. | 灯泡通电发光放热 | B. | 活性炭吸附水中的异味 | ||
| C. | 干冰用于人工降雨 | D. | 石墨制成金刚石 |
9.某同学做氧化铜与稀硫酸反应的实验,操作示意图如下,其中操作有错误的是( )
| A. |  加入氧化铜 | B. |  倾倒稀硫酸 | ||
| C. |  加热反应物 | D. |  洗涤试管 |
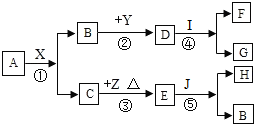 如图是中学常见的物质的转换关系图.其中A,B常温下都为无色液体,且组成元素相同,A,B,X,Y,E都为氧化物,X,E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,请回答:
如图是中学常见的物质的转换关系图.其中A,B常温下都为无色液体,且组成元素相同,A,B,X,Y,E都为氧化物,X,E都为黑色固体,Y可用作干燥剂,F是大理石的主要成分,请回答: 水是人类最宝贵的自然资源,依据所学化学知识回答:
水是人类最宝贵的自然资源,依据所学化学知识回答: