题目内容
15. 氧气是一种化学性质比较活泼的气体,它能与许多物质发生反应.
氧气是一种化学性质比较活泼的气体,它能与许多物质发生反应.(1)如图,铁丝在氧气中燃烧,集气瓶中水的作用是防止生成物熔化溅落炸裂瓶底;
(2)现有0.8克硫与氧气充分反应,理论上需要分解高锰酸钾多少克?
(2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑)
(3)二氧化硫气体对人体有毒,会污染大气,可用氢氧化钠溶液吸收,二氧化硫的化学性质与二氧化碳相似,写出二氧化硫与氢氧化钠反应的化学方程式SO2+2NaOH=Na2SO3+H2O.
分析 (1)根据铁丝燃烧时的注意事项分析回答;
(2)根据硫的质量利用反应的方程式求出氧气的质量,再根据氧气的质量求出高锰酸钾的质量;
(3)根据二氧化硫与氢氧化钠反应生成亚硫酸钠和水解答.
解答 解:(1)铁丝燃烧时盛氧气的集气瓶底少量水的作用是:防止生成的高温熔融物溅落瓶底引起集气瓶底炸裂;
(2)设理论上需要分解高锰酸钾的质量为x,由S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑可得
S~O2~2KMnO4
32 316
0.8g x
$\frac{32}{0.8g}=\frac{316}{x}$
x=7.9g
方法二:
设需要氧气的质量为x
S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2
32 32
0.8g x
$\frac{32}{0.8g}=\frac{32}{x}$
x=0.8g
设理论上需要分解高锰酸钾的质量为y
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
y 0.8g
$\frac{316}{y}=\frac{32}{0.8g}$
y=7.9g
(3)二氧化硫与氢氧化钠反应的化学方程式为:SO2+2NaOH=Na2SO3+H2O
答案:
(1)防止生成物熔化溅落炸裂瓶底;
(2)理论上需要分解高锰酸钾7.9g;
(3)SO2+2NaOH=Na2SO3+H2O.
点评 提醒同学们除了要认真实验,观察细致,还要明确实验中操作的意图.

练习册系列答案
相关题目
17.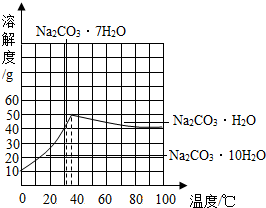 碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3•10H2O、Na2CO3•7H2O和Na2CO3•H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )
碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3•10H2O、Na2CO3•7H2O和Na2CO3•H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )
 碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3•10H2O、Na2CO3•7H2O和Na2CO3•H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )
碳酸钠从溶液里结晶析出时,晶体里总是结合着一定数目的水分子(结晶水),随温度变化可分别得到Na2CO3•10H2O、Na2CO3•7H2O和Na2CO3•H2O三种晶体.分析碳酸钠溶解度随温度变化曲线(见图)得到的下列说法,正确的是( )| A. | 随温度升高,碳酸钠的溶解度逐渐增大 | |
| B. | 碳酸钠从溶液结晶析出时,没有发生化学反应 | |
| C. | 碳酸钠溶液在高温条件下结晶,析出的晶体是Na2CO3•H2O | |
| D. | 碳酸钠溶液在低温条件下结晶,析出的晶体主要是Na2CO3•7H2O |
18.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
①H ②Fe2+ ③Cu ④P2O5 ⑤Fe3+⑥NaCl.
| A. | 能表示一个分子的是①④⑥ | |
| B. | 表示物质组成的化学式是③④⑥ | |
| C. | ②⑤的质子数相同,化学性质也相同 | |
| D. | ④中的数字“5”表示五氧化二磷中有5个氧原子 |
3.下列实验不能达到目的是( )
| A. | 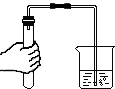 检查气密性 | B. | 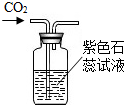 验证CO2性质 | ||
| C. | 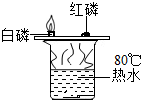 验证燃烧需O2 | D. | 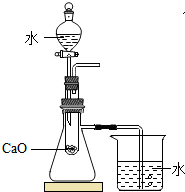 验证反应放热 |
10.某校化学兴趣小组同学探究发现:铜绿[Cu2(OH)2CO3]受热分解后,除生成CO2和水蒸气外,试管中还有一些黑色粉末状固体.请回答下列问题:
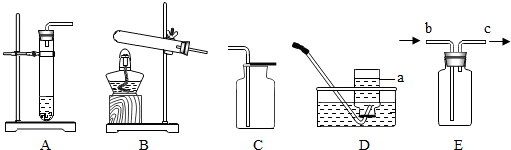
(1)写出标号a的仪器名称集气瓶.
(2)实验室分解铜绿选用的发生装置为B(填序号).初中实验室制取CO2$\underset{收}{•}\underset{集}{•}\underset{装}{•}\underset{置}{•}$也可用E(长进短出),试分析其原因:二氧化碳的密度比空气大.
(3)若向澄清的石灰水中通入少量CO2,可观察到的现象:澄清石灰水变浑浊.用化学方程式表达:Ca(OH)2+CO2═CaCO3↓+H2O.
(4)充分反应后,兴趣小组对试管中的黑色粉末状状固体进一步探究
a.[提出问题]黑色固体是什么?
b.[猜想与假设]黑色固体可能是:Ⅰ.氧化铜Ⅱ.炭粉Ⅲ.氧化铜与炭粉.
c.[查阅资料]炭粉和氧化铜均为黑色固体.炭粉不与稀酸反应,也不溶于稀酸.而氧化铜可与稀酸反应而溶解.
d.[设计实验方案]向试管中的黑色固体滴加足量的试剂为A(填序号)
(A.H2SO4 B.NaOH C.NaCl D.H2O),完成下列实验报告:
如果猜想Ⅰ正确,猜想Ⅰ所发生反应的化学方程式为:H2SO4+CuO=CuSO4+H2O.

(1)写出标号a的仪器名称集气瓶.
(2)实验室分解铜绿选用的发生装置为B(填序号).初中实验室制取CO2$\underset{收}{•}\underset{集}{•}\underset{装}{•}\underset{置}{•}$也可用E(长进短出),试分析其原因:二氧化碳的密度比空气大.
(3)若向澄清的石灰水中通入少量CO2,可观察到的现象:澄清石灰水变浑浊.用化学方程式表达:Ca(OH)2+CO2═CaCO3↓+H2O.
(4)充分反应后,兴趣小组对试管中的黑色粉末状状固体进一步探究
a.[提出问题]黑色固体是什么?
b.[猜想与假设]黑色固体可能是:Ⅰ.氧化铜Ⅱ.炭粉Ⅲ.氧化铜与炭粉.
c.[查阅资料]炭粉和氧化铜均为黑色固体.炭粉不与稀酸反应,也不溶于稀酸.而氧化铜可与稀酸反应而溶解.
d.[设计实验方案]向试管中的黑色固体滴加足量的试剂为A(填序号)
(A.H2SO4 B.NaOH C.NaCl D.H2O),完成下列实验报告:
| 实验现象 | 实验结论 |
| 黑色固体全部溶解,溶液呈蓝色 | 猜想Ⅰ正确 |
| 猜想Ⅱ正确 | |
| 猜想Ⅲ正确 |
20.铝合金、氧化铝、硫酸铝三种物质的分类正确的是( )
| A. | 混合物、氧化物、盐 | B. | 单质、混合物、盐 | ||
| C. | 盐、氧化物、纯净物 | D. | 混合物、盐、化合物 |
7.下列关于物质性质及用途的描述中,错误的是( )
| A. | 碳具有还原性,可冶炼金属 | |
| B. | 氧气具有氧化性,可作为燃料 | |
| C. | 氮气的化学性质稳定,可作为保护气 | |
| D. | 石灰石受热分解,可用于制备生石灰 |
4.实验室部分装置如图所示,请回答下列问题.

(1)选择发生和收集O2的装置,填写在下表中(填字母).
(2)如果用MnO2与浓H2SO4加热制备O2,可选用的发生装置是C(填字母).
(3)选用F装置收集气体时,下列实验操作正确的是①②③(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若需制备3.2g O2,至少需要消耗31.6g KMnO4.(已知KMnO4的相对分子质量为158)

(1)选择发生和收集O2的装置,填写在下表中(填字母).
| 选用药品 | 发生装置 | 收集装置 |
| H2O2溶液、MnO2 | B | D或F |
| KMnO4 | A |
(3)选用F装置收集气体时,下列实验操作正确的是①②③(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若需制备3.2g O2,至少需要消耗31.6g KMnO4.(已知KMnO4的相对分子质量为158)
5.“绿色化学”有助于解决环境污染问题,下列做法不符合“绿色化学”理念的是( )
| A. | 因地制宜,大力发展风力发电 | B. | 废旧电池集中回收,并填埋处理 | ||
| C. | 大力发展公共交通,提倡绿色出行 | D. | 使用可降解塑料,减少“白色污染” |