题目内容
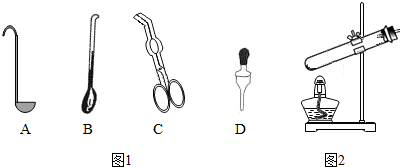
4.实验室部分装置如图所示,请回答下列问题.
(1)选择发生和收集O2的装置,填写在下表中(填字母).
| 选用药品 | 发生装置 | 收集装置 |
| H2O2溶液、MnO2 | B | D或F |
| KMnO4 | A |
(3)选用F装置收集气体时,下列实验操作正确的是①②③(填序号).
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体后,将集气瓶盖上玻璃片再移出水槽
(4)实验室用KMnO4制备O2的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若需制备3.2g O2,至少需要消耗31.6g KMnO4.(已知KMnO4的相对分子质量为158)
分析 (1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;氧气的密度比空气的密度大,不易溶于水;
(2)根据反应物的状态和反应条件可以选择实验装置;
(3)利用排水法收集气体要注意一些问题;
(4)根据反应的化学方程式和生成氧气的质量可以计算反应的高锰酸钾的质量.
解答 解:(1)利用过氧化氢制取氧气不需要加热,应该用B装置作为发生装置;利用高锰酸钾制取氧气需要加热,应该用A装置作为发生装置;因为氧气的密度比空气大,可以用向上排空气法收集,即用D装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集.
故填:B;A;D或F.
(2)如果用MnO2与浓H2SO4加热制备O2,可选用的发生装置是C装置.
故填:C.
(3)选用F装置收集气体时,
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中,该选项说法正确;
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶,该选项说法正确;
③收集气体后,将集气瓶盖上玻璃片再移出水槽,该选项说法正确.
故填:①②③.
(4)实验室用KMnO4制备O2的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
设需要高锰酸钾的质量为x,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
316 32
x 3.2g
$\frac{316}{x}$=$\frac{32}{3.2g}$,
x=31.6g,
故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;31.6.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 阅读快车系列答案
阅读快车系列答案| A. |  尼龙背包 | B. |  塑料瓶 | C. |  陶瓷花盆 | D. |  手机塑料外壳 |
| A. | 用聚乙烯塑料制得食品袋 | B. | 用食盐制得纯碱 | ||
| C. | 将液态空气分离制得氧气 | D. | 将石油分离制得汽油 |
查阅资料:CO2+Zn$\frac{\underline{\;\;△\;\;}}{\;}$CO+ZnO;FeCl3溶液遇KSCN溶液变红.

请回答下列问题:
(1)仪器a的名称是酒精灯,装置B的作用是除去多余的二氧化碳,尾气处理的方法是点燃或收集.
(2)将研究小组分为两组,按如图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(纯净物).两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) | 溶解,有气泡,溶液呈浅绿色 |
| 2 | 取步骤1所得溶液,滴加KSCN溶液 | 变红 | 无现象 |
(3)从安全考虑,本实验应在装置A和B之间添加装置E防止倒吸.(填字母编号)
(4)该对比实验结果表明CO的还原能力随温度的升高而增强(填“增强”或“减弱”).
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
②写出上述反应的化学反应方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明相同条件下,反应物浓度越大,反应速率越快.
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,同学分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.

| A. | 用装置甲溶解固体 | B. | 用装置乙进行过滤 | ||
| C. | 用装置丙蒸发滤液 | D. | 用装置丁称量固体 |
 控制变量法是学习化学常用的方法.下面是探究燃烧条件的实验,请你根据实验图示和资料回答有关问题.
控制变量法是学习化学常用的方法.下面是探究燃烧条件的实验,请你根据实验图示和资料回答有关问题. 氧气是一种化学性质比较活泼的气体,它能与许多物质发生反应.
氧气是一种化学性质比较活泼的气体,它能与许多物质发生反应. 盐酸是一种重要的化工产品,也是实验室中重要的化学试剂.
盐酸是一种重要的化工产品,也是实验室中重要的化学试剂. H+,
H+, Cl-,
Cl-, Fe2+.
Fe2+.