题目内容
13.小明在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.[探究目的]探究所得溶液的酸碱性.
[提出猜想]所得溶液可能呈酸性,也可能呈中性,还可能呈酸性.
[实验验证]
| 实验操作 | 实验现象 | 结 论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 若无色酚酞试液变红色. | 溶液呈碱性; |
| 若无色酚酞试液变不色. | 溶液呈中性或酸性; |
(1)用pH试纸可以粗略地测出溶液的酸碱度.
(2)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小明对所得溶液进行了如下处理:向溶液中逐滴加入硫酸铜溶液,并发生了反应,直到不产生沉淀为止.然后过滤,把滤液倒入蒸发皿进行加热蒸发溶剂,得到NaCl晶体.上述产生沉淀的化学方程式CuSO4+2NaOH═Cu(OH)2↓+Na2SO4.
(3)若无色酚酞试液变不色,为了进一步确定溶液的酸碱性,小明提出了以下方案:
方案一:取样,加入Na2CO3溶液,若观察到有气泡产生,则所取的溶液呈酸性;若无明显现象,则溶液呈中性.
方案二:取样,加入铁屑,若有大量气泡产生,则所取的溶液呈酸性;该反应的化学方程式为Fe+2HCl═FeCl2+H2↑;若无明显现象,则溶液呈中性.
方案三:…
分析 氢氧化钠溶液呈碱性,能使酚酞变红,盐酸呈酸性,氢氧化钠与盐酸反应生成氯化钠和水,呈中性,在酸性和中性溶液中酚酞不变色,氢氧化钠能与某些物质反应生成沉淀,碳酸盐遇酸化气,活泼金属能与酸反应生成氢气.
解答 解:[提出猜想]盐酸与氢氧化钠混合,会发生反应,由于酸碱的量不固定故溶液可能呈碱性、中性或酸性,所以本题答案为:中,酸性;
[实验验证]酚酞在碱性溶液中变红,在酸性和中性溶液中为无色,所以本题答案为:
| 实验操作 | 实验现象 | 结论 |
| 红 | ||
| 中 酸 |
(1)人们用pH来表示溶液酸碱性的强弱程度,用pH试纸可以测定溶液的酸碱度,所以本题答案为:pH试纸.
(2)溶液呈碱性的实质是氢氧根离子的缘故,氢氧化钠能与硫酸铜反应生成氢氧化铜沉淀和硫酸铜,所以本题答案为:OH-;CuSO4+2NaOH═Cu(OH)2↓+Na2SO4;
(3)所取溶液呈酸性,与碳酸钠接触能产生二氧化碳,所以本题答案为:有气泡产生;
所取溶液呈酸性,则能与铁反应生成氢气,所以本题答案为:Fe+2HCl═FeCl2+H2↑.
点评 本题考查了酸碱中和反应以及酸的检验方法,完成此题,可以依据物质的性质进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法错误的是( )


| A. | 甲物质的溶解度随温度的升高而增大 | |
| B. | 在t1℃时,甲、乙两物质的溶解度相等 | |
| C. | 将乙物质的饱和溶液从t2降到t1有晶体析出 | |
| D. | 在t1℃时,用100g水配成的乙物质饱和溶液中溶质的质量是25g |
4.下列各组物质中,前者为氧化物、后者为混合物的是( )
| A. | 臭氧、冰水 | B. | 干冰、石灰浆 | C. | 氯酸钾、水银 | D. | 硫酸、加碘盐 |
1. 在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成份为生石灰”(如图).小明将其拿出来放置一段时间后,发现纸袋内的白色颗粒黏在一起成为块状.他感到好奇,认为生石灰样品已经变质了.于是他对里面的成分进行实验探究.请你参与讨论并完成以下实验报告.
在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成份为生石灰”(如图).小明将其拿出来放置一段时间后,发现纸袋内的白色颗粒黏在一起成为块状.他感到好奇,认为生石灰样品已经变质了.于是他对里面的成分进行实验探究.请你参与讨论并完成以下实验报告.
【提出问题】变质后的生石灰样品中有哪些主要成分?
【作出猜想】样品中除了还有部分没变质的CaO外;
甲同学猜想变质生成Ca(OH)2;
乙同学猜想变质生成CaCO3;
你认为变质得到的物质还可能是Ca(OH)2和CaCO3.
【实验与结论】请你通过实验验证你的猜想:
【拓展与应用】小组同学反思了生石灰变质的原因,认识到实验室应密封保存生石灰.
 在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成份为生石灰”(如图).小明将其拿出来放置一段时间后,发现纸袋内的白色颗粒黏在一起成为块状.他感到好奇,认为生石灰样品已经变质了.于是他对里面的成分进行实验探究.请你参与讨论并完成以下实验报告.
在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成份为生石灰”(如图).小明将其拿出来放置一段时间后,发现纸袋内的白色颗粒黏在一起成为块状.他感到好奇,认为生石灰样品已经变质了.于是他对里面的成分进行实验探究.请你参与讨论并完成以下实验报告.【提出问题】变质后的生石灰样品中有哪些主要成分?
【作出猜想】样品中除了还有部分没变质的CaO外;
甲同学猜想变质生成Ca(OH)2;
乙同学猜想变质生成CaCO3;
你认为变质得到的物质还可能是Ca(OH)2和CaCO3.
【实验与结论】请你通过实验验证你的猜想:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量的变质样品于烧杯 中,加足量的水,充分溶解后过滤. ②向滤液中加入适量浓的碳酸 钠溶液. ③向滤出固体中加入适量 稀盐酸溶液. | 步骤②中产生有白色沉淀产生, 反应的化学方程式:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH; 步骤③中的现象固体溶解,有气泡产生. | 你的猜想正确 |
8.在CuCl2和AlCl3的混合溶液中,加入过量的铁粉,充分反应后过滤,留在滤纸上的物质是( )
| A. | Cu | B. | Cu和Al | C. | Fe和Cu | D. | Cu、Al和Fe |
14.为了鉴别一桶实验室用的蒸馏水是否被某种酸污染,下列不可采用的方法是( )
| A. | 取样品少许用PH试纸测定样品的pH值 | |
| B. | 取样品滴入酚酞试液观察颜色是否发生变化 | |
| C. | 加入少量金属锌,看是否产生气泡 | |
| D. | 取样品滴入紫色石蕊试液观察颜色变化 |
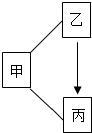 甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
甲、乙、丙是初中化学中常见的物质,其转化关系如图所示(反应条件已省 略).若乙是相对分子质量最小的氧化物,甲、乙均由两种相同的元素组成,请写出实验室由甲制取丙的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.