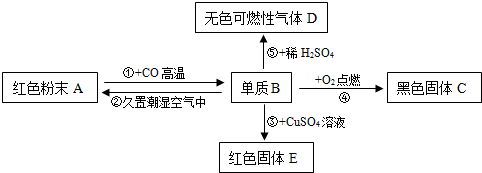
题目内容
在反应A+2B=C+2D中,9.8g A与8g B完全反应,生成14.2g C,则下列结论正确的是( )
| A、生成D1.8g |
| B、质量比为49:40:71:18 |
| C、生成D7.2g |
| D、相对分子质量比98:80:142:36 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律进行分析,由题意9.8gA与8gB完全反应生成14.2gC,可求出反应生成的D的质量,进而计算出各物质的质量比,根据各物质的质量比,再根据化学方程式可求出各物质的相对分子质量之比.
解答:解:A、由题意可知,9.8gA与8gB完全反应生成14.2gC,根据质量守恒定律可出D的质量为9.8g+8g-14.2g=3.6g,故错误;
B、根据A中计算可以知道A、B、C、D的质量比为9.8g:8g:14.2g:3.6g=49:40:71:18,故正确.
C、根据A中计算可以知道生成D的质量为3.6g,故错误;
D、根据B中的计算可以知道,A、B、C、D的质量比为9.8g:8g:14.2g:3.6g=49:40:71:18,根据化学方程式的意义可以知道A:2B:C:2D=9.8g:8g:14.2g:3.6g,所以A、B、C、D的相对分子质量比不等于98:80:142:36,故错误.
故选B.
B、根据A中计算可以知道A、B、C、D的质量比为9.8g:8g:14.2g:3.6g=49:40:71:18,故正确.
C、根据A中计算可以知道生成D的质量为3.6g,故错误;
D、根据B中的计算可以知道,A、B、C、D的质量比为9.8g:8g:14.2g:3.6g=49:40:71:18,根据化学方程式的意义可以知道A:2B:C:2D=9.8g:8g:14.2g:3.6g,所以A、B、C、D的相对分子质量比不等于98:80:142:36,故错误.
故选B.
点评:本题主要考查学生运用质量守恒定律进行推断的能力,需认真分析,找出质量关系,就可以求解.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
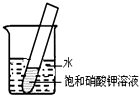 如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的( )
如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的( )| A、氢氧化钠固体 | B、生石灰固体 |
| C、硝酸铵 | D、浓硫酸 |
在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下:下列说法正确的是( )
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 6 | 111 | 4 |
| 反应后质量/g | 待测 | 15 | 0 | 84 |
| A、该反应中A、B、C、D四种物质(参加反应或生成)的质量比为26:9:111:80 |
| B、反应后密闭容器中A的质量为22 g |
| C、该闭容器中发生的化学变化属于分解反应 |
| D、密闭容器中发生的化学变化属于化合反应 |
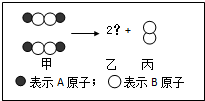 如图,二分子的甲反应生成二分子的乙与一分子的丙,已知甲、乙、丙三者为不同的纯净物,则乙物质的化学式为下列哪一项( )
如图,二分子的甲反应生成二分子的乙与一分子的丙,已知甲、乙、丙三者为不同的纯净物,则乙物质的化学式为下列哪一项( )| A、A2 |
| B、AB2 |
| C、A2B |
| D、A4B2 |
 某同学为了测定一种补钙保健食品中CuCO3的质量分数,(其包装说明如图所示)进行了如下实验:将100片该食品研碎后放入一烧杯中,向其中慢慢滴加稀盐酸,直到不再产生气泡时,共消耗稀盐酸200g,(该保健食品中其它成分不与盐酸反应)并测得烧杯内剩余物质的总质量为232.4g.请你根据以上数据计算:
某同学为了测定一种补钙保健食品中CuCO3的质量分数,(其包装说明如图所示)进行了如下实验:将100片该食品研碎后放入一烧杯中,向其中慢慢滴加稀盐酸,直到不再产生气泡时,共消耗稀盐酸200g,(该保健食品中其它成分不与盐酸反应)并测得烧杯内剩余物质的总质量为232.4g.请你根据以上数据计算: