题目内容
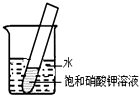 如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的( )
如图所示,20℃时,将盛有饱和KNO3溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是下列中的( )| A、氢氧化钠固体 | B、生石灰固体 |
| C、硝酸铵 | D、浓硫酸 |
考点:晶体和结晶的概念与现象,溶解时的吸热或放热现象,生石灰的性质与用途
专题:溶液、浊液与溶解度
分析:根据已有的知识进行分析分析解答,硝酸钾的溶解度随温度的降低而减小,要使硝酸钾结晶析出,可以使温度降低,据此解答.
解答:解:要使硝酸钾结晶析出,可以使温度降低,
A、氢氧化钠固体溶于水放热,使温度升高,错误;
B、生石灰与水反应放热,使温度升高,错误;
C、硝酸铵溶于水吸收热量,使温度降低,正确;
D、浓硫酸溶于水放热,使温度升高,错误;
故选C.
A、氢氧化钠固体溶于水放热,使温度升高,错误;
B、生石灰与水反应放热,使温度升高,错误;
C、硝酸铵溶于水吸收热量,使温度降低,正确;
D、浓硫酸溶于水放热,使温度升高,错误;
故选C.
点评:本题考查的是物质溶于水时的吸放热现象,掌握常见物质的溶于水时的能量变化是解答本题的关键.

练习册系列答案
相关题目
下列实验操作,正确的是( )
①用托盘天平称取5.6g氧化铜粉末
②实验用剩的药品要放回原瓶,以免浪费药品
③用排水集气法可得到比较纯净的氧气
④用10mL量筒量取8.2mL水.
①用托盘天平称取5.6g氧化铜粉末
②实验用剩的药品要放回原瓶,以免浪费药品
③用排水集气法可得到比较纯净的氧气
④用10mL量筒量取8.2mL水.
| A、只有①④ | B、①②④ |
| C、①③④ | D、只有②③ |
在反应A+2B=C+2D中,9.8g A与8g B完全反应,生成14.2g C,则下列结论正确的是( )
| A、生成D1.8g |
| B、质量比为49:40:71:18 |
| C、生成D7.2g |
| D、相对分子质量比98:80:142:36 |
 如图为探究空气中氧气含量的实验:
如图为探究空气中氧气含量的实验:

 ,该元素原子核内有
,该元素原子核内有