题目内容
10.一包不纯的Na2CO3固体,杂质可能是CuSO4、KNO3、CaCl2、NaHCO3中的一种或几种.现取该样品溶于水得到无色澄清溶液,另取样品10.6g,加入100g稀硫酸恰好完全反应,产生气体4.6g,则下列判断正确的是( )| A. | 样品中一定没有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 样品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 样品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶质的质量分数不大于9.8% |
分析 根据题干提供的信息进行分析解答即可,得到无色溶液,则一定不会含有硫酸铜,加硫酸反应生成二氧化碳气体,碳酸钠能与硫酸反应生成气体,根据10.6g纯净的碳酸钠生成气体的质量,确定物质的成分,据此解答.
解答 解:由于溶液是无色,故一定不会含有硫酸铜,又有碳酸钠能与氯化钙反应产生白色沉淀,故一定不会含有氯化钙;
10.6g纯净的碳酸钠生成二氧化碳质量
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 98 44
10.6g 9.8g 4.4g
现在生成二氧化碳的质量大于4.4g,故一定含有碳酸氢钠,硝酸钾无法确定是否含有;由于生成二氧化碳的质量大于4.4g,故硫酸的质量分数一定大于9.8%,
A、样品中一定没有CuSO4、CaCl2,一定有NaHCO3,正确;
B、样品中不一定含有KNO3,一定含有NaHCO3,错误;
C、样品中一定含有NaHCO3,可能含有KNO3,正确;
D、所加的稀硫酸溶质的质量分数大于9.8%,错误;
故选AC.
点评 本题考查的是混合物成分的推断,完成此题,可以依据已有的物质的性质以及物质间反应的质量关系进行.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
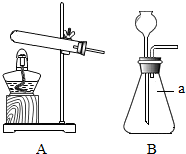
20.根据如图中的实验装置,回答问题:
(1)写出图B中仪器a的名称:锥形瓶.
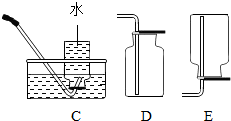
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,发生和收集装置为A、C(或D)(填字母).
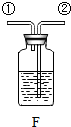
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的②端口(填“①”或“②”)通入,F中发生的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室用加热氯酸钾和二氧化锰混合物制取氧气的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,发生和收集装置为A、C(或D)(填字母).
(3)实验室用石灰石和稀盐酸反应制取二氧化碳,其中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的F装置来除去,则混合气体应从F装置的②端口(填“①”或“②”)通入,F中发生的化学方程式为NaHCO3+HCl═NaCl+H2O+CO2↑.
2. 甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
 甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| B. | t1℃时,甲饱和溶液溶质质量分数为50% | |
| C. | 甲的溶解度大于乙的溶解度 | |
| D. | 甲溶液中混有少量乙可通过降温结晶进行提纯 |
19.下列物质中,有一种物质能跟另外3种物质发生反应,这种物质是( )
| A. | Ca(OH)2 | B. | Na2CO3 | C. | Fe2O3 | D. | HCl |


