题目内容
2. 甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃时,甲、乙两种物质的溶液中,溶质质量分数相等 | |
| B. | t1℃时,甲饱和溶液溶质质量分数为50% | |
| C. | 甲的溶解度大于乙的溶解度 | |
| D. | 甲溶液中混有少量乙可通过降温结晶进行提纯 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、t1℃时,甲、乙两种物质的溶解度相等,所以饱和溶液中,溶质质量分数相等,故A错误;
B、t2℃时,甲物质饱和溶液的质量分数为:$\frac{50g}{150g}$×100%=33.3%,所以t1℃时,甲饱和溶液溶质质量分数小于50%,故B错误;
C、在比较物质的溶解度时,需要指明温度,故C错误;
D、甲物质的溶解度受温度变化影响较大,所以甲溶液中混有少量乙可通过降温结晶进行提纯,故D正确.
故选:D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
12.明确宏观现象的微观本质是学习化学的重要思想方法.下列说法正确的是( )
| A. | 水与酒精混合液的体积小于混合前二者体积之和,是因为混合后分子体积变小 | |
| B. | 水结成冰,是因为温度降低,分子停止运动 | |
| C. | 水通电分解生成氢气和氧气,是因为水中含有氢分子和氧分子 | |
| D. | 水与冰的共存物是纯净物,是因为它们由同种分子构成 |
10.一包不纯的Na2CO3固体,杂质可能是CuSO4、KNO3、CaCl2、NaHCO3中的一种或几种.现取该样品溶于水得到无色澄清溶液,另取样品10.6g,加入100g稀硫酸恰好完全反应,产生气体4.6g,则下列判断正确的是( )
| A. | 样品中一定没有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 样品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 样品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶质的质量分数不大于9.8% |
7.下列有关实验现象的描述,正确的是( )
| A. | 镁条在空气中燃烧发出蓝紫色火焰,产生大量白烟 | |
| B. | 电解水正极一侧得到的气体能使带火星的木条复燃 | |
| C. | 铜丝放入足量稀硫酸中产生大量气泡,溶液变蓝 | |
| D. | 打开浓硫酸的试剂瓶盖时,瓶口有白雾产生 |
14.下列变化中属于化学变化的是( )
| A. | 酒精挥发 | B. | 铁钉生锈 | C. | 冰雪融化 | D. | 西瓜榨汁 |
8.下列四个图象分别表示对应的四种操作过程,其中表示正确的图象是( )

| A. | 加热高锰酸钾固体至质量不再减轻 | |
| B. | 向pH=13的氢氧化钠溶液中逐滴加入pH=1的硫酸溶液 | |
| C. | 某温度下,向一定量的水中加入食盐并不断搅拌 | |
| D. | 将等质量的锌、铁分别加入到足量的稀硫酸中,充分反应 |
9.除去下列各物质中混有的少量杂质,所有试剂、方法正确的是( )
| 序号 | 物质 | 杂质 | 试剂、方法 |
| A | CO2 | CO | 点燃 |
| B | CaO | CaCO3 | 适量稀盐酸,过滤 |
| C | MgCl2溶液 | 盐酸 | 适量的氢氧化钠溶液 |
| D | CO | CO2 | 足量的氢氧化钠溶液、浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
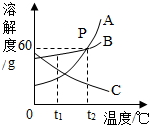 如(1)t2℃时,向70gA物质中加入100g水,充分溶解后,所得溶液是(填“是”或“不是”)饱和溶液,该溶液的溶质质量分数是37.5%;
如(1)t2℃时,向70gA物质中加入100g水,充分溶解后,所得溶液是(填“是”或“不是”)饱和溶液,该溶液的溶质质量分数是37.5%;