题目内容
18.把7g黄铜(黄铜是Cu-Zn的合金)放在盛有100g稀硫酸的烧杯中,恰好完全反应.反应后烧杯中剩余物质的总质量是106.8g.(1)根据质量守恒定律,反应后生成的氢气质量是0.2g.
(2)求该黄铜中锌的质量分数.
分析 (1)烧杯中总物质前后减少的质量为氢气的质量;
(2)利用锌和硫酸反应的化学方程式,根据氢气的质量求出锌的质量,进而求出黄铜中锌的质量分数.
解答 解:(1)由质量守恒定律可知氢气的质量=7g+100g-106.8g=0.2g.
(2)设锌的质量为x,生成硫酸锌的质量为y.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.2g
$\frac{65}{x}=\frac{2}{0.2g}$
x=6.5g
该黄铜中锌的质量分数=$\frac{6.5g}{7g}×$100%≈92.9%
(1)质量守恒;0.2;
(2)该黄铜中锌的质量分数为92.9%
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,关键之处是能够分析出反应前后物质的质量之差是生成氢气的质量.

练习册系列答案
相关题目
6.下列图示的实验操作正确的是( )
| A. | 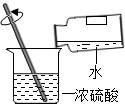 稀释浓硫酸 | B. |  测定溶液的pH | ||
| C. |  过滤 | D. | 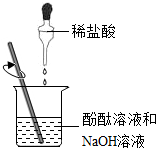 验证酸碱中和反应 |
10.一包不纯的Na2CO3固体,杂质可能是CuSO4、KNO3、CaCl2、NaHCO3中的一种或几种.现取该样品溶于水得到无色澄清溶液,另取样品10.6g,加入100g稀硫酸恰好完全反应,产生气体4.6g,则下列判断正确的是( )
| A. | 样品中一定没有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 样品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 样品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶质的质量分数不大于9.8% |
7.下列有关实验现象的描述,正确的是( )
| A. | 镁条在空气中燃烧发出蓝紫色火焰,产生大量白烟 | |
| B. | 电解水正极一侧得到的气体能使带火星的木条复燃 | |
| C. | 铜丝放入足量稀硫酸中产生大量气泡,溶液变蓝 | |
| D. | 打开浓硫酸的试剂瓶盖时,瓶口有白雾产生 |
5.逻辑推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 离子都带电,所以带电的微粒一定是离子 | |
| B. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 | |
| C. | 单质中只含有一种元素,所以只含有一种元素的物质一定是单质 | |
| D. | 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 |
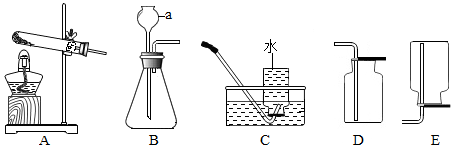
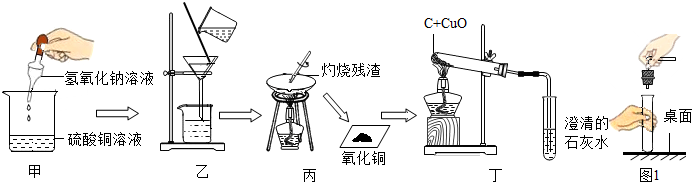
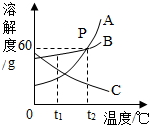 如(1)t2℃时,向70gA物质中加入100g水,充分溶解后,所得溶液是(填“是”或“不是”)饱和溶液,该溶液的溶质质量分数是37.5%;
如(1)t2℃时,向70gA物质中加入100g水,充分溶解后,所得溶液是(填“是”或“不是”)饱和溶液,该溶液的溶质质量分数是37.5%;