题目内容
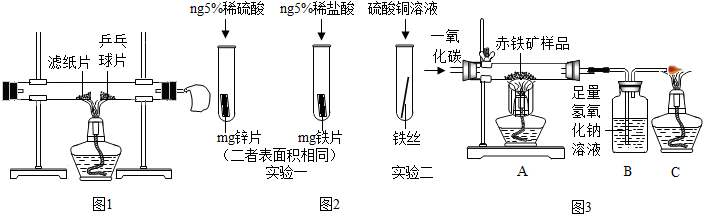
15.请回答下列与金属有关的问题.(1)生铁片与纯铁片相互刻画时,在纯铁片片表面会留下划痕.
(2)为了防止月饼变质,常在月饼的内包装袋中放入一小包防腐剂,它的主要成分是铁粉,铁粉的作用是与氧气发生反应,防止月饼因氧化而变质并且能吸水防潮.
(3)向AgNO3和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤,向滤渣中加盐酸有气泡,则滤渣中一定含有的金属是Ag、Cu、Zn.
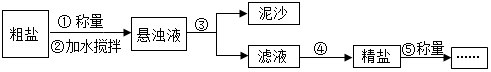
(4)为了达到收旧利废的目的,欲从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料MgSO4和有关金属,其主要实验过程如下,请回答:

①步骤①中被磁铁吸引的金属A是铁(或Fe).
②步骤③的操作是过滤.
③步骤②所涉及的化学方程式为Mg+H2SO4=MgSO4+H2↑.
(5)将7.3g已部分氧化的锌粉,加入到98g10%的稀硫酸中,恰好完全反应.则所得溶液中溶质的质量为C(填序号).
A.14.5g B.5.5g C.16.1g D.18.1g.
分析 (1)合金要比组成成分的金属的硬度大;(2)铁生锈需要与氧气和水接触考虑;(3)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,利用此知识分析即可;(4)根据题目给出的信息:铁能够被磁铁吸引,因此A是铁;镁和铜的混合物中,加入适量的稀硫酸,镁和硫酸反应生成硫酸镁和氢气,铜不反应,因此过滤可以得到B,即金属铜;(5)根据反应的方程Zn+H2SO4═ZnSO4+H2↑、ZnO+H2SO4═ZnSO4+H2O、找出硫酸与硫酸锌之间的关系式进行计算.
解答 (1)合金要比组成成分的金属的硬度大,生铁片与纯铁片相比,生铁片硬度大,纯铁硬度小,所以相互刻画时,在纯铁片表面会留下划痕.
(2)铁生锈需要与氧气和水接触,所以常在月饼的内包装袋中放入一小包防腐剂铁粉,铁粉的作用是与氧气发生反应,防止月饼因氧化而变质并且能吸水防潮;
(3)在金属活动性顺序中,锌>氢>铜>银,锌能与硝酸银反应生成银和硝酸锌,可以和硝酸铜反应生成铜和硝酸锌;所以放入锌后,锌要先置换出硝酸银中银,再去置换硝酸同种的铜,所以如果向滤渣中加盐酸有气泡,则滤渣中一定含有锌,即加入的锌过量,所以银和铜都被置换出来了,所以滤渣中含有铜、锌、银;
(4)①铁能够被磁铁吸引,因此A是铁;镁和铜的混合物中,加入适量的稀硫酸,镁和硫酸反应生成硫酸镁和氢气,铜不反应,因此过滤可以得到B,即金属铜;
②硫酸镁溶液蒸发结晶即可得到硫酸镁固体;
③步骤②是镁和硫酸反应生成硫酸镁和氢气,其化学方程式为:Mg+H2SO4=MgSO4+H2↑
(5)解:设所得溶液中溶质的质量为x,由Zn+H2SO4═ZnSO4+H2↑、ZnO+H2SO4═ZnSO4+H2O 得:
H2SO4~ZnSO4
98 161
98g×10% x
根据:$\frac{98}{161}=\frac{98g×10%}{x}$解得:x=16.1g
由以上计算可知,A、B、D错误,C正确
故答案为:(1)纯铁片
(2)与氧气发生反应,防止月饼因氧化而变质并且能吸水防潮
(3)Ag、Cu、Zn (4)铁(或Fe);过滤;Mg+H2SO4=MgSO4+H2↑(5)C.
点评 本考点属于物质的制备,做本类题型时,要注意题目给出的信息,利用已知条件来解决有关的问题.本题考查了金属的化学性质,还有酸碱盐的化学性质,综合性比较强,要认真掌握.

| A. | 制取少量NaOH溶液:将Ca(OH)2溶液和NaCl溶液混合,过滤 | |
| B. | 检验NaOH溶液和盐酸反应后的溶液中是否有盐酸:取样,滴加AgNO3溶液 | |
| C. | 分离CaCl2和MgCl2的固体:溶解后,加入适量Ca(OH)2溶液,充分反应后过滤,蒸发 | |
| D. | 验证Cu的活动性比Ag强:将Ag丝伸入Cu(NO3)2溶液中,观察表面及溶液颜色是否变化 |
| A. | 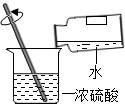 稀释浓硫酸 | B. |  测定溶液的pH | ||
| C. |  过滤 | D. | 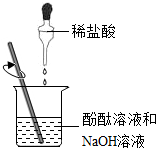 验证酸碱中和反应 |
| A. | 样品中一定没有CuSO4、CaCl2,一定有NaHCO3 | |
| B. | 样品中一定含有KNO3,可能含有NaHCO3 | |
| C. | 样品中一定含有NaHCO3,可能含有KNO3 | |
| D. | 所加的稀硫酸溶质的质量分数不大于9.8% |
| A. | 水通电分解 | B. | 物体热胀冷缩 | ||
| C. | 小苏打治疗胃酸过多 | D. | 浓硫酸使蔗糖变黑 |
| A. | 镁条在空气中燃烧发出蓝紫色火焰,产生大量白烟 | |
| B. | 电解水正极一侧得到的气体能使带火星的木条复燃 | |
| C. | 铜丝放入足量稀硫酸中产生大量气泡,溶液变蓝 | |
| D. | 打开浓硫酸的试剂瓶盖时,瓶口有白雾产生 |