题目内容
9. 某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )
某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )| A. | 属于单质 | B. | 它里面的氮原子静止不动 | ||
| C. | 原子之间存在间隔 | D. | 它的结构与C60相同 |
分析 根据分子、原子、离子等微粒的性质:之间有间隔,不断运动,质量和体积都很小进行解答.
解答 解:A、由不同种元素组成的纯净物属于化合物,这个新型材料是由碳、氮两种元素组成的,故属于化合物,故选项错误;
B、分子、原子、离子都是不断的运动的,故选项错误;
C、微粒之间有间隔,故选项正确;
D、它的结构与C60不相同,C60中没有氮原子,故选项错误;
故选C
点评 本题考查了物质的分类、微粒的性质等知识,题目较易.

练习册系列答案
相关题目
19.某学校化学活动小组的同学,取刚降地面的雨水样,用pH计(测pH的仪器)每隔几分钟测一次pH,其数据如表所示:
(1)绘制时间-pH关系图

(2)在测定的时间内,酸雨的酸性是增强(填增强或减弱).
(3)煤中含有的硫在燃烧时会以二氧化硫的形式排放,污染大气.
①硫在空气中燃烧的化学方程式是S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2;
②回收二氧化硫可以生产硫酸,化学方程式为2SO2+O2+2H2O═2H2SO4.参加反应的SO2与生成的H2SO4的质量比是32:49,将6.4t的SO2全部转化,可得到H2SO4的质量为9.8t.
| 测定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |

(2)在测定的时间内,酸雨的酸性是增强(填增强或减弱).
(3)煤中含有的硫在燃烧时会以二氧化硫的形式排放,污染大气.
①硫在空气中燃烧的化学方程式是S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2;
②回收二氧化硫可以生产硫酸,化学方程式为2SO2+O2+2H2O═2H2SO4.参加反应的SO2与生成的H2SO4的质量比是32:49,将6.4t的SO2全部转化,可得到H2SO4的质量为9.8t.
20. 蛋白质是构成细胞的基本物质,α-丙氨酸是构成人体蛋白的氨基酸之一,如图是α-丙氨酸的分子结构模型图,下列对α-丙氨酸的叙述正确的是( )
蛋白质是构成细胞的基本物质,α-丙氨酸是构成人体蛋白的氨基酸之一,如图是α-丙氨酸的分子结构模型图,下列对α-丙氨酸的叙述正确的是( )
 蛋白质是构成细胞的基本物质,α-丙氨酸是构成人体蛋白的氨基酸之一,如图是α-丙氨酸的分子结构模型图,下列对α-丙氨酸的叙述正确的是( )
蛋白质是构成细胞的基本物质,α-丙氨酸是构成人体蛋白的氨基酸之一,如图是α-丙氨酸的分子结构模型图,下列对α-丙氨酸的叙述正确的是( )| A. | α-丙氨酸中碳、氢元素的质量比为3:7 | |
| B. | α-丙氨酸分子中含有3个碳原子 | |
| C. | α-丙氨酸分子的质子数和中子数不相等 | |
| D. | α-丙氨酸是由四种原子构成的有机物 |
4.下列有关资源、能源的叙述正确的是( )
| A. | 可利用的淡水资源只占全球水储量的30.4% | |
| B. | 煤的综合利用可以得到煤油、煤焦油、柴油等有用的物质 | |
| C. | 空气的稀有气体的质量分数约为0.94% | |
| D. | 宝贵的金属资源主要分布于地壳和海洋中 |
14.下表是NaCl、KNO3在不同温度时的溶解度,下列说法不正确的是( )
| 温度 | 0 | 10 | 20 | 30 | 40 | 50 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | |
| A. | 20℃时,将100gKNO3饱和溶液蒸发10g水析出3.16g晶体 | |
| B. | KNO3与NaCl在某温度下溶解度相同,其溶解度数值在36.0~36.3之间 | |
| C. | 20℃时可以配制36%的NaCl溶液 | |
| D. | KNO3中含有少量NaCl,可以降温结晶提纯KNO3 |
 图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息回答下列问题.
图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息回答下列问题.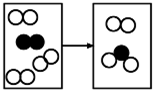 如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子.
如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子. B.
B. C.
C.
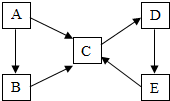 已知A、B、C、D、E五种物质均为初中化学常见物质,都含有同一种元素,它们之间的转化关系如图所示.
已知A、B、C、D、E五种物质均为初中化学常见物质,都含有同一种元素,它们之间的转化关系如图所示.