题目内容
17.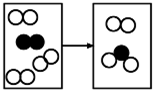 如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子.
如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子.(1)反应后方框内应再填入1个C微粒.
A.
 B.
B. C.
C.
(2)由此反应可知分子与原子主要不同之处是在化学反应中分子可以分,原子不能再分.
分析 (1)根据质量守恒反应前后原子的种类、原子的数目分析应填入的粒子;
(2)根据微粒的变化分析分子与原子主要不同之处.
解答 解:(1)根据质量守恒定律,化学反应前后原子的种类、个数不变,因此填入在反应后填入一个C微粒后该反应正好遵循质量守恒定律.
(2)从图示中微粒的变化可知,分子与原子主要不同之处是:在化学反应中分子可以分,原子不能再分.
故答案为:(1)C;(2)在化学反应中分子可以分,原子不能再分.
点评 此题是对化学反应的微观过程的考查,解题的关键是依据已有的化学反应实质和结合图示物质的结构进行.

练习册系列答案
相关题目
8.下列变化过程中只发生了物理变化的是( )
| A. | 波尔多液腐蚀铁制容器 | |
| B. | 霓虹灯填充稀有气体,通电时发出不同颜色的光 | |
| C. | 用液氯对自来水消毒杀菌 | |
| D. | 酸碱指示剂遇酸碱溶液时变色 |
9. 某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )
某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )
 某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )
某新型材料是由60个碳原子组成的笼状结构(如图所示),里面还装着一个氮原子,这种材料能安装在移动设备上的原子钟.下列关于这种材料的说法正确的是( )| A. | 属于单质 | B. | 它里面的氮原子静止不动 | ||
| C. | 原子之间存在间隔 | D. | 它的结构与C60相同 |
5.钠原子的结构示意图为 ,下列有关说法错误的是( )
,下列有关说法错误的是( )
 ,下列有关说法错误的是( )
,下列有关说法错误的是( )| A. | 钠原子核外有三个电子层 | B. | 钠离子的结构示意图为  | ||
| C. | 钠原子核内有11个质子 | D. | 氧化钠的化学式为Na2O |
9. 将一定质量的红磷在一瓶氧气中充分燃烧,其固体质量随时间的变化可用如图表示,则用(M2-M1)表示的质量是( )
将一定质量的红磷在一瓶氧气中充分燃烧,其固体质量随时间的变化可用如图表示,则用(M2-M1)表示的质量是( )
 将一定质量的红磷在一瓶氧气中充分燃烧,其固体质量随时间的变化可用如图表示,则用(M2-M1)表示的质量是( )
将一定质量的红磷在一瓶氧气中充分燃烧,其固体质量随时间的变化可用如图表示,则用(M2-M1)表示的质量是( )| A. | 生成P2O5的质量 | B. | 参加反应的O2的质量 | ||
| C. | 参加反应的红磷的质量 | D. | 剩余的O2的质量 |
6.下列方案中,不合理的是( )
| A. | 除去氢气中的水蒸气可用浓硫酸 | |
| B. | 清洗玻璃仪器上的油污可用热的纯碱溶液 | |
| C. | 分离NaCl、CaCO3的混合物,可用溶解、过滤、蒸发 | |
| D. | 验证质量守恒定律,可称量锌与稀硫酸反应前后溶液的质量 |

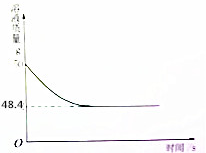 双氧水是过氧化氢的水溶液,它由杀菌消毒的作用,国家标准H2O2的质量百分含量不低于3%,小军从家中拿来一瓶医用过氧化氢溶液.和同学们一起测定溶质质量分数,他们取出该溶液50g,加入适量二氧化锰2g,反应后溶液的质量与反应时间的关系如图所示.
双氧水是过氧化氢的水溶液,它由杀菌消毒的作用,国家标准H2O2的质量百分含量不低于3%,小军从家中拿来一瓶医用过氧化氢溶液.和同学们一起测定溶质质量分数,他们取出该溶液50g,加入适量二氧化锰2g,反应后溶液的质量与反应时间的关系如图所示.