题目内容
7.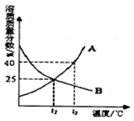 如图是A、B两种物质在不同温度下溶解于水形成的饱和溶液的溶质质量分数的曲线,下列说法正确的是( )
如图是A、B两种物质在不同温度下溶解于水形成的饱和溶液的溶质质量分数的曲线,下列说法正确的是( )| A. | t1温度下,等质量的A、B两种溶液中所含的溶质质量一定相等 | |
| B. | A中混有少量B可用降温结晶的方法提纯A | |
| C. | t2温度下A的溶解度一定大于B,且A的溶解度为40克 | |
| D. | 在t2温度下能分别配制25%的A、B两种溶液 |
分析 根据题目中的曲线判断出物质的溶解度,然后分析溶液的组成情况,结合选项进行解答.
解答 解:A、t1温度下,A、B物质的溶解度相等,所以等质量的A、B两种溶液中所含的溶质质量一定相等,故A正确;
B、A物质的溶质质量分数随温度的升高而增大,所以溶解度也随温度的升高而增大,B物质的溶质质量分数随温度的升高而减小,所以溶解度随温度的升高而减小,所以A中混有少量B可用降温结晶的方法提纯A,故B正确;
C、t2温度下A的溶质质量分数大于B,A的溶质质量分数是40%,溶解度不一定为40克,故C错误;
D、在t2温度下,B物质的溶质质量分数小于25%,所以不能配制25%B溶液,故D错误.
故选:AB.
点评 本题难度不大,主要考查了A、B两种物质的饱和溶液的质量百分比浓度(溶质质量分数)随温度变化的曲线,通过本题可以培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
17.下列实验不能成功的是( )
| A. | 用熟石灰鉴别氯化铵和氯化钾 | B. | 用食盐水制作叶脉书签 | ||
| C. | 用水鉴别硝酸铵和氯化钠 | D. | 用肥皂水鉴别硬水与软水 |
18.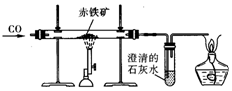 小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )
小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )
(温馨提示:杂质不参加反应)
 小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )
小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )(温馨提示:杂质不参加反应)
| A. | 玻璃管中的固体由黑色逐渐变成红色 | |
| B. | 剩余固体7.6g是得到的铁的质量 | |
| C. | 生成CO2的质量为2.4 g | |
| D. | 铁矿石样品中Fe2O3的质量分数为80% |
15.草木灰是一种碱性农家肥,下列肥料不能用与草木灰混合的是( )
| A. | KNO3 | B. | NH4HCO3 | C. | KCl | D. | Ca(PO4)2 |
2.实验室有200g碳酸银样品(杂质既不溶于水,也不与酸反应),与500g氢元素质量分数为10.5%的稀盐酸恰好完全反应,过滤,得到205.5g固体,则该 样品中碳酸银的质量分数为( )
| A. | 23% | B. | 46% | C. | 69% | D. | 92% |
12.课本中的图表、模型等都能提供很多信息.下面有关说法错误的是( )
| A. | 根据“平衡膳食宝塔图”,可分析自己日常饮食结构的合理性 | |
| B. | 根据“常见物质密度表”,可比较相同质量的水、酒精的体积大小 | |
| C. | 根据“酸、碱和盐溶解性表”,可判断两种物质在某温度时的溶解度大小 | |
| D. | 根据“溶解度曲线”,可以分析获得晶体的方法 |
 如图所示的是有关物质的转化关系(部分反应物、生成物和反应条件已省略).已知乙为碳不完全燃烧时的产物,丙为植物光合作用的产物,丁俗称纯碱.请回答下列问题:
如图所示的是有关物质的转化关系(部分反应物、生成物和反应条件已省略).已知乙为碳不完全燃烧时的产物,丙为植物光合作用的产物,丁俗称纯碱.请回答下列问题: