题目内容
18.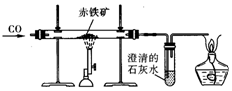 小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )
小文同学利用下图实验装置测定某赤铁矿石样品中Fe2O3的质量分数,取10g样品与足量CO充分反应后,测得剩余固体的质量为7.6g,下列说法正确的是( )(温馨提示:杂质不参加反应)
| A. | 玻璃管中的固体由黑色逐渐变成红色 | |
| B. | 剩余固体7.6g是得到的铁的质量 | |
| C. | 生成CO2的质量为2.4 g | |
| D. | 铁矿石样品中Fe2O3的质量分数为80% |
分析 A、氧化铁在加热时被一氧化碳还原成铁,同时生成二氧化碳,玻璃管中的固体由红色逐渐变黑;对于B、C、D三个选项可以通过化学方程式来进行求算,然后做出判断.
解答 解:A、氧化铁在加热时被一氧化碳还原成铁,同时生成二氧化碳,玻璃管中的固体由红色逐渐变黑,故错误;
B、剩余7.6g固体是生成的铁与杂质的总质量,故错误;
C、设反应生成二氧化碳的质量为x,则由化学方程式可知,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2?固体质量减少
160 112 132 160-112=48
x 10g-7.6g=2.4g
$\frac{132}{48}=\frac{x}{2.4g}$
x=6.6g
故错误;
D、根据B的分析可以求出消耗氧化铁的质量为:2.4g÷$\frac{16×3}{160}×100%$=8g,故氧化铁的质量分数为:$\frac{8g}{10g}$×100%=80%,故正确.
故选D.
点评 本题综合性较强,较全面的考查了一氧化碳还原氧化铁,尤其是利用数据对混合物的判断增加了试题难度,掌握反应前后元素的质量不变,并会结合方程式分析即可顺利解答.

(1)市售的一种罐装饮料,在饮料罐的夹层中分别装入_种固体物质和水,饮用前摇动饮料罐使它们混合,饮料温度就会降低,这种固体物质可能是C(填字母).
A.烧碱 B.食盐 C.硝酸铵 D.生石灰
(2)下表是硝酸钾、氯化钠在不同温度下的溶解度表 (单位:g/100g水)
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.6 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
②30℃时,硝酸钾的溶解度是45.8g;
③KNO3溶液中含有少量NaCl时,可通过降温结晶的方法提纯;
④对③析出的晶体和剩余溶液描述正确的是A(填写编号).
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定不含有NaCl
C.剩余的溶液一定是纯净物 D.析出的晶体中只含有KNO3.
| A. | -1 | B. | +1 | C. | +5 | D. | +7 |
| A. | 用熟石灰改良酸性土壤 | B. | 用含氢氧化铝的药物治疗胃酸过多 | ||
| C. | 用熟石灰配制农药波尔多液 | D. | 用氨水(NH3•H2O)处理工厂的硫酸 |
| 次数 | 一 | 二 | 三 | 四 | 五 |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 | 25 |
| 剩余固体的质量/g | 9.6 | 6.7 | 3.8 | 0.9 | 0.9 |
(2)该23200t这样的铁矿石理论上能冶炼得到铁的质量为10393.6t.
(3)求加入稀盐酸恰好完全反应时所得溶液的溶质质量分数?(结果保留到0.1%)
| A. | 薄荷脑属于有机物 | B. | 薄荷脑的相对分子质量为156g | ||
| C. | 1个薄荷脑分子中含有31个原子 | D. | 薄荷脑中碳元素的质量分数最大 |
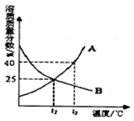 如图是A、B两种物质在不同温度下溶解于水形成的饱和溶液的溶质质量分数的曲线,下列说法正确的是( )
如图是A、B两种物质在不同温度下溶解于水形成的饱和溶液的溶质质量分数的曲线,下列说法正确的是( )| A. | t1温度下,等质量的A、B两种溶液中所含的溶质质量一定相等 | |
| B. | A中混有少量B可用降温结晶的方法提纯A | |
| C. | t2温度下A的溶解度一定大于B,且A的溶解度为40克 | |
| D. | 在t2温度下能分别配制25%的A、B两种溶液 |
| A. |  | B. |  | C. |  | D. |  |