题目内容
1.结合如图1所示实验装置,回答下列问题.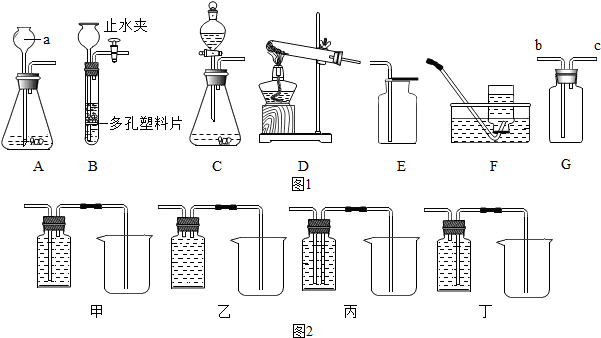
(1)写出图中标号仪器的名称:a长颈漏斗;
(2)实验室选用D装置制取氧气,其反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
二氧化锰是该反应的催化剂,为了从反应后的剩余物中回收二氧化锰,实验操作为溶解、过滤、洗涤干燥.
(3)实验室制取氢气时,选用B装置为发生装置的优点是控制反应的发生和停止,选择的收集装置是F(或G)(填序号).
(4)某同学用G装置收集二氧化碳,验满的方法是将燃着的木条放在导管C处,木条熄灭则满;
若用C装置制取二氧化碳,打开如图装置中分液漏斗的活塞后,水不能滴下,该同学认为整套装置不漏气,你认为他的判断不正确(填“正确”或“不正确”);实验室为了除去其中的氯化氢气体,并将剩余气体收集在集气瓶中,下列装置中最为合理的是丙装置(填序号),左边试剂瓶中盛放的试剂是图2中的饱和碳酸氢钠溶液.
分析 (1)据常用仪器回答;
(2)D装置属于固体加热型,试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,二氧化锰是反应的催化剂,二氧化锰不溶于水,氯化钾易溶于水,所以可用过滤的方法回收二氧化锰;
(3)据B装置特点分析其优越性,并据氢气的密度和溶解性选择收集装置;
(4)验满二氧化碳的方法是将燃着的木条平放在集气瓶口,观察木条是否熄灭进行判断;打开如图装置中分液漏斗的活塞后,水不能滴下,该同学认为整套装置不漏气,他的判断不正确,因为分液漏斗上有盖,因此水不能滴下;实验室为了除去其中的氯化氢气体,并将剩余气体收集在集气瓶中,下列装置中最为合理的是丙装置,左边试剂瓶中盛放的试剂是饱和碳酸氢钠溶液.
解答 解:(1)长颈漏斗方便加液体药品;
(2)B装置属于固体加热型,试管口无棉花,说明是用加热氯酸钾和二氧化锰混合物的方法制取氧气,反应方程式是:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,其中二氧化锰做催化剂,二氧化锰不溶于水,氯化钾易溶于水,所以可用过滤的方法回收二氧化锰,步骤为溶解、过滤、洗涤干燥;
(3)实验室制取氢气时,选用B装置为发生装置的优点是:可通过止水夹随时控制反应的发生和停止,氢气密度比空气小、难溶于水,所以可用排水法或向下排空气法收集;
(4)某同学用G装置收集二氧化碳,因为二氧化碳密度比空气大,所以应从长管进气,导管排气,验满的方法是将燃着的木条放在导管C处,木条熄灭则满;若用C装置制取二氧化碳,打开如图装置中分液漏斗的活塞后,水不能滴下,该同学认为整套装置不漏气,他的判断不正确,因为分液漏斗上有盖,因此水不能滴下,无法据此现象判断是否漏气;实验室为了除去其中的氯化氢气体,并将剩余气体收集在集气瓶中,下列装置中最为合理的是丙装置,左边试剂瓶中盛放的试剂是饱和碳酸氢钠溶液,可与氯化氢气体反应,而不与二氧化碳反应;
故答案为:(1)长颈漏斗;
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;催化剂;过滤;
(3)控制反应的发生和停止; F(或G);
(4)将燃着的木条放在导管C处,木条熄灭则满;不正确;丙;饱和碳酸氢钠溶液.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的验满和除杂等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 阅读快车系列答案
阅读快车系列答案| 实验次数 | 1 | 2 | 3 | 4 |
| 每次加入样品的质量/g | 5 | 5 | 5 | 5 |
| 反应后剩余物质的总质量/g | 40.4 | 44.3 | m | 54.3 |
| 生成CO2质量/g | 1.1 | 1.1 | 0 | 0 |
(1)表格数据显示,盐酸在第次反应中耗尽;
(2)表格中m的数值为.
(3)请计算烧碱样品中NaOH的质量分数.
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
| A. | 工业中利用活性炭脱色以制白糖 | |
| B. | CO2 能使被石蕊染成紫色的干花变红 | |
| C. | 在一定条件下将石墨转化为金刚石发生了化学变化 | |
| D. | CO具有还原性,CO2具有氧化性 |
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】猜想I:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH和Na2CO3.
【实验与探究】
(1)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钙溶液. | 实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立. 过程中发生反应的化学方程式:CaCl2+Na2CO3=BaCO3↓+2NaCl |
(3)小华同学对实验(1)的方案提出了质疑,他认为该方案的操作步骤中应该改进的是加入过量的氯化钡溶液.
(4)小明又提出了一个定量实验方案:通过测定产生沉淀的质量来证明猜想II或III成立.实验如下:准确称取mg固体样品于试管中,加蒸馏水完全溶解,然后滴加足量氯化钙溶液,充分反应后过滤、洗涤、干燥称得沉淀的质量为ng,若猜想III成立,则m与n的关系式为(用含m和n的等式或不等式表示)m=$\frac{106n}{197}$.
(5)你还有其它定量实验方法来证明猜想II或猜想III成立吗?写出方案即可.取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加总量氯化钡溶液.实验过程中产生白色沉淀,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
| A. | 物质都是由原子和分子构成的 | |
| B. | 化学变化的基础是分子中原子的重新组合 | |
| C. | 门捷列夫发现了元素周期律并编制出元素周期表 | |
| D. | 化学在劳动人民与自然界的种种灾难进行的斗争中不断发展. |
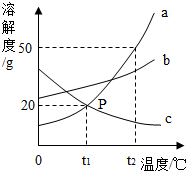 如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点
如图所示是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点