题目内容
14.A-G是初中常见的7种物质,它们有如图所示的转化关系,已知A、V组成元素相等,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.
(1)请写出下列物质的化学符号:DC,GSO2,HH2;
(2)请写出下列反应的符号表达式:
①B→FC+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
②C→B+H2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
③请指出C→B+H的化学反应类型分解反应.
分析 A-G是初中常见的7种物质,已知A、V组成元素相等,B、F、G是无色气体,结合过氧化氢在二氧化锰的催化作用下生成水和氧气,水通电分解生成氢气和氧气,则A为过氧化氢,B为氧气,C为水,H为氢气;其中大量排放F会引起温室效应,则F为二氧化碳;D是黑色固体,碳在氧气中燃烧生成二氧化碳,D为碳;E在纯净的B中燃烧发出明亮的蓝紫色火焰,结合硫在氧气中燃烧发出明亮的蓝紫色火焰,则E为硫,G为二氧化硫;据此进行分析解答.
解答 解:A-G是初中常见的7种物质,已知A、V组成元素相等,B、F、G是无色气体,由过氧化氢在二氧化锰的催化作用下生成水和氧气,水通电分解生成氢气和氧气,则A为过氧化氢,B为氧气,C为水,H为氢气;其中大量排放F会引起温室效应,则F为二氧化碳;D是黑色固体,碳在氧气中燃烧生成二氧化碳,D为碳;E在纯净的B中燃烧发出明亮的蓝紫色火焰,结合硫在氧气中燃烧发出明亮的蓝紫色火焰,则E为硫,G为二氧化硫.
(1)D、G、H的化学式分别是C、SO2、H2.
(2)①B→F,即碳在氧气中燃烧生成二氧化碳,反应的化学方程式为:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
②C→B+H,即水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
③C→B+H,即水通电分解生成氢气和氧气,该反应符合“一变多”的特征,属于分解反应.
故答案为:(1)C、SO2、H2;(2)①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;②2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;③分解反应.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案| A. | 水 | B. | 氧气 | C. | 金刚石 | D. | 硫酸铜 |
| 相 关 说 法 | 解 释 | |
| A | 夏季垃圾堆的气味比冬季的大 | 温度升高,分子运动加快 |
| B | 石灰水、稀硫酸都能导电 | 酸碱溶液中都存在带电的粒子 |
| C | 稀盐酸、氯化钠溶液都能与硝酸银溶液反应 | 溶液中都有氯离子 |
| D | 敞口放置的浓盐酸会变稀 | 分子之间有间隔 |
| A. | A | B. | B | C. | C | D. | D |
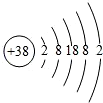 据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答:
据《自然》杂志报道,科学家最近研究出一种以锶(Sr)做钟摆的钟,它是世界上最精确的钟,锶的原子结构示意图如图所示,请回答: