题目内容
6.用稀硫酸和玉米芯反应可制得重要的化工原料糖醛,糖醛的化学式为C5H4O2.(1)糖醛中氢氧原子个数比为2:1;
(2)糖醛的相对分子质量为96.
分析 (1)根据1个糖醛分子的构成,进行分析解答.
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
解答 解:(1)1个糖醛分子中含有4个氢原子和2个氧原子,则糖醛中氢、氧原子个数比为4:2=2:1.
(2)糖醛的相对分子质量为12×5+1×4+16×2=96.
故答案为:(1)2:1;(2)96.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下表是某地区市场销售的一种“加碘食盐”包装上的部分文字说明.请根据下表,结合所学知识.回答下列问题.
(1)碘酸钾的化学式为KI03,则碘酸钾的相对分子质量为214,其中碘元素的质量分 数约为59.3%,碘元素的化合价为+5.
(2)根据加碘食盐的贮存指南和食用方法,可推测出碘酸钾的化学性质之一为易氧化、见光分解、易潮解
(3)从2000年10月1日起,我国食盐加碘含量调整为每千克食盐中含碘0.035g,相当于每千克食盐中约含碘酸钾0.059g.
| 配料表 | 精制食盐、碘酸钾 |
| 含碘量 | 20-40mg |
| 包装日期 | 见封底 |
| 贮存指南 | 密封、避光、防潮 |
| 食用方法 | 烹饪时,待食品熟后加入食盐 |
(2)根据加碘食盐的贮存指南和食用方法,可推测出碘酸钾的化学性质之一为易氧化、见光分解、易潮解
(3)从2000年10月1日起,我国食盐加碘含量调整为每千克食盐中含碘0.035g,相当于每千克食盐中约含碘酸钾0.059g.
1.某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
①为探究催化剂种类对氯酸钾分解速率的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与 1.0g MnO2均匀混合加热
Ⅱ.将3.0g KClO3与 x g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的文字或符号表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;Ⅱ中x的值应为1.0.
②乙探究了影响双氧水分解速率的某种因素.实验数据记录如下:
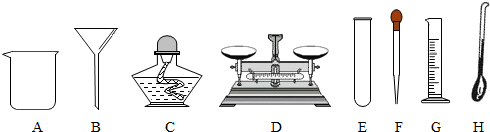
本实验中,测量O2体积的装置是(图1)c(填编号).

实验结论:在相同条件下,双氧水浓度越大,双氧水分解得越快.丙用图2装置进行实验,通过比较相同时间天平读数差值大小(其它合理也可)也能达到实验目的.
①为探究催化剂种类对氯酸钾分解速率的影响,甲设计以下对比实验:
Ⅰ.将3.0g KClO3与 1.0g MnO2均匀混合加热
Ⅱ.将3.0g KClO3与 x g CuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的文字或符号表达式是过氧化氢$\stackrel{二氧化锰}{→}$水+氧气或2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;Ⅱ中x的值应为1.0.
②乙探究了影响双氧水分解速率的某种因素.实验数据记录如下:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

实验结论:在相同条件下,双氧水浓度越大,双氧水分解得越快.丙用图2装置进行实验,通过比较相同时间天平读数差值大小(其它合理也可)也能达到实验目的.
18.有100g溶质质量分数为10%的硝酸钾溶液,若将其浓度变为20%,可以采用的方法是( )
| A. | 蒸发掉溶剂的$\frac{1}{2}$ | B. | 加入10g的硝酸钾 | ||
| C. | 蒸发掉50g水 | D. | 加入12.5g 硝酸钾 |