题目内容
15.有一种工业废水,其中含有大量硝酸锌和少量硝酸银.某同学设计了一个既经济又合理的实验方案,制备硝酸锌固体并回收银.方案流程如下:
回答下列问题:
(1)操作I中用到的玻璃仪器有烧杯、漏斗和玻璃棒.
(2)操作I中需加入的物质是锌,目的是将硝酸硬溶液中的银全部置换出来.
(3)Y为稀硫酸;乙与硝酸钡反应的化学方程式为ZnSO4+Ba(NO3)2=BaSO4↓+Zn(NO3)2.
(4)操作Ⅱ的操作是蒸发浓缩、结晶、过滤.
分析 过滤分离不溶性固体与液体,向含有大量硝酸锌和少量硝酸银加入过量的锌将硝酸银的银全部置换出来,过滤得到锌和银的混合物和滤液硝酸锌,然后在固体混合物中加入适量硫酸与锌反应生成硫酸锌溶液,再加入适量的硝酸钡将硫酸根离子除去,得到硝酸锌的溶液,最后将硝酸锌溶液蒸发浓缩、结晶、过滤即可.
解答 解:由题意可知,向含有大量硝酸锌和少量硝酸银加入过量的锌将硝酸银的银全部置换出来,过滤得到锌和银的混合物和滤液硝酸锌,然后在固体混合物中加入适量硫酸与锌反应生成硫酸锌溶液,再加入适量的硝酸钡将硫酸根离子除去,得到硝酸锌的溶液,最后将硝酸锌溶液蒸发浓缩、结晶、过滤即可.
(1)步骤①是将固体与溶液分离,故可用过滤,过滤操作中用到的玻璃仪器是烧杯、漏斗、玻璃棒;
(2)由上述分析可知,操作I中需加入的物质是锌,目的是将将硝酸硬溶液中的银全部置换出来.
(3)Y为稀硫酸;乙为硫酸与锌反应生成的硫酸锌,与硝酸钡反应的化学方程式为:ZnSO4+Ba(NO3)2=BaSO4↓+Zn(NO3)2.
(4)操作Ⅱ的操作是蒸发浓缩、结晶、过滤.
故答案为:(1)玻璃棒;(2)锌;将硝酸硬溶液中的银全部置换出来;(3)ZnSO4+Ba(NO3)2=BaSO4↓+Zn(NO3)2;(4)结晶.
点评 从废水中回收金属一般步骤先加入一种廉价金属置换出另一种金属,然后过滤,将过量金属除去即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.试管是初中实验中最常见的仪器,试管口的朝向不同,在实验中的应用也不同.下列有关说法错误的是( )
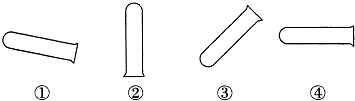

| A. | ①的放置方向,是在加热固体时 | |
| B. | ②的放置方向,是在试管刷洗后 | |
| C. | ③的放置方向,是在加热少量液体时 | |
| D. | ④的放置方向,是向试管里倾倒液体时 |
3.下列物质中既存在离子又存在分子的是( )
| A. | 碳酸钠固体 | B. | 金刚石 | C. | 蔗糖溶液 | D. | 稀硫酸 |
7.镁在二氧化碳中燃烧,可生成碳和氧化镁.该反应中Mg、CO2、C、MgO的质量比为( )
| A. | 12:11:3:20 | B. | 24:44:12:40 | C. | 6:11:3:10 | D. | 12:22:6:20 |
4.蒸馒头时,常在发酵的面团里加人一些纯碱溶液,其作用是( )
| A. | 除去发酵生成的酸 | B. | 产生二氧化碳,使馒头膨大 | ||
| C. | 使馒头变白 | D. | 既除去生成的酸,又使馒头膨大 |