题目内容
14.海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等.综合利用海水制备金属镁的流程如图所示:
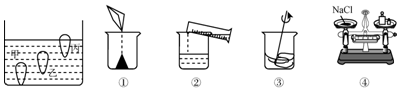
〔1〕操作a的名称是过滤,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、漏斗.
〔2〕写出第②步反应的化学方程式CaO+H2O═Ca(OH)2
写出第③步反应的化学方程式Mg(OH)2+2HCl═MgCl2+2H2O.
分析 根据已有的知识进行分析,贝壳的主要成分是碳酸钙,过滤是分离不溶性固体和液体的方法,该实验操作中使用的玻璃仪器有烧杯、漏斗和玻璃棒,氧化钙能与水反应生成氢氧化钙,氢氧化镁能和盐酸反应生成氯化镁和水以及基本的反应类型进行解答.
解答 解:(1)过滤是分离不溶性固体和液体的方法,所以操作a的名称是过滤;在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、漏斗;故填:过滤;漏斗;
(2)氧化钙和水反应生成氢氧化钙,反应的化学方程式为CaO+H2O═Ca(OH)2;故填:CaO+H2O═Ca(OH)2;
氢氧化镁能和盐酸反应生成氯化镁和水,反应的化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O.故填:Mg(OH)2+2HCl═MgCl2+2H2O.
点评 故填:Mg(OH)2+2HCl═MgCl2+2H2O.本题考查的是物质制备的知识,完成此题,可以依据物质的性质进行.

练习册系列答案
相关题目
2.为适应不同人群的需要,市场上供应的食盐除碘盐外还有无碘竹盐、低钠盐和健康平衡盐等.现有两种品牌的食盐A和B,主要成分的含量见表:
(注:两种食盐仅NaCl中含有钠元素;35.1g/100g表示每100g食盐中含钠元素质量为35.1g)
(1)加碘盐是通过加入KIO3的方法制成的,KIO3中碘元素的化合价为+5.
(2)NaCl中钠元素质量分数以39%计,则100克食盐A中氯化钠的质量是90克,100克食盐B中钠元素的质量是36.27克.
| 食盐种类 | 食盐A | 食盐B |
| 主要成分的含量 | (以钠元素质量计) 35.1g/100g | (以NaCl质量计) 93.0g/100g |
(1)加碘盐是通过加入KIO3的方法制成的,KIO3中碘元素的化合价为+5.
(2)NaCl中钠元素质量分数以39%计,则100克食盐A中氯化钠的质量是90克,100克食盐B中钠元素的质量是36.27克.
6.下列图示所示的装置气密性检查的操作中,表明装置漏气的是( )
| A. |  | B. | 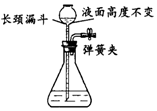 | ||
| C. | 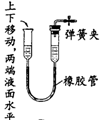 | D. |  |
4.配制硝酸钾溶液时得到如表数据,根据表中数据分析不正确的是( )
| 序号 | 温度/℃ | 水的质量/克 | 所加硝酸钾质量/克 | 所得溶液的质量/克 |
| ① | 28 | 10 | 4 | 14 |
| ② | 28 | 10 | 6 | 15 |
| ③ | 60 | 10 | 8 | 18 |
| A. | ①②所得溶液中的溶质得溶解度相同 | |
| B. | 60℃时等质量水中能溶解硝酸钾比28℃多 | |
| C. | 28℃时10克水最多能溶解5克硝酸钾 | |
| D. | ②中硝酸钾的溶解度为50克 ③中硝酸钾得溶解度为80克 |

 A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)
A、B两种化合物的溶解度曲线如图.现要用结晶法从A、B混和物中提取A.(不考虑A、B共存时,对各自溶解度的影响.)