题目内容
19.根据有关燃烧与灭火的知识回答下列问题:(1)把蜡烛放在空气中,蜡烛没有燃烧,原因是温度没有达到着火点;
(2)使燃料充分燃烧可以节约资源并减少对空气的污染.增大燃料与空气的接触面积和提供充足的氧气都有利于燃料的充分燃烧;
(3)从发生火灾的房间中逃生的正确方法为用湿毛巾捂住口鼻沿墙根伏低身子爬向门.
分析 (1)根据燃烧必须满足:物质具有可燃性、达到物质的着火点、与氧气接触分析;
(2)氧气越充分,燃烧越剧烈;
(3)根据火场逃生的措施来分析.
解答 解:(1)蜡烛放在空气中,与氧气(空气)接触,蜡烛没有燃烧,原因是温度没有达到着火点.故答案为:温度没有达到着火点;
(2)增大燃料与空气的接触面和提供充足的氧气,有利于燃料的充分燃烧.故答案为:氧气;
(3)从发生火灾的房间中逃生的正确方法为用湿毛巾捂住口鼻沿墙根伏低身子爬向门外;故填:用湿毛巾捂住口鼻沿墙根伏低身子爬向门(其他合理答案均可).
点评 燃烧的条件是:可燃物、与氧气接触、达到着火点,三者缺一不可;另外氧气越充分,燃烧越剧烈.

练习册系列答案
相关题目
9.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如右表所示).他从瓶中倒出100毫升用于配制成稀硫酸,问
(1)这100毫升浓硫酸的质量为184克,其中含溶质硫酸180.32克.
(2)欲配制100毫升质量分数为20%的稀硫酸(密度为1.14克每立方厘米),需要多少毫升这种浓硫酸和多少毫升水?
| 浓硫酸(H2SO4)500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克/厘米3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
(2)欲配制100毫升质量分数为20%的稀硫酸(密度为1.14克每立方厘米),需要多少毫升这种浓硫酸和多少毫升水?
10.金属Ni、Zn分别放入其他三种金属盐X、Y、Z的溶液中,置换反应的结果,有无金属析出的情况如下:
它们的金属活动性递减的顺序是X>Zn>Y>Ni>Z.
| X盐 | Y盐 | Z盐 | |
| Ni | 无 | 无 | 有 |
| Zn | 无 | 有 | 有 |
4.给试管中的液体加热时,若出现试管破裂的现象,其原因不可能是( )
| A. | 加热前试管外壁有水 | B. | 加热不均匀,局部温度过高 | ||
| C. | 试管内的液体超过 $\frac{1}{3}$ | D. | 试管触及灯芯了 |
8.下列说法中正确的是( )
| A. | 在100g水里最多能溶解36g食盐,所以食盐的溶解度为36g | |
| B. | 所有固体物质的溶液度都随着温度的升高而增大 | |
| C. | 有过剩溶质存在于其中的溶液,一定是这种物质在该温度时的饱和溶液 | |
| D. | 20℃时100g水里溶解了30g硝酸钾,所以硝酸钾的溶质质量分数为30% |
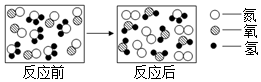

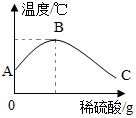 学习酸碱中和反应时,很多同学对其产生了探究兴趣
学习酸碱中和反应时,很多同学对其产生了探究兴趣