题目内容
16.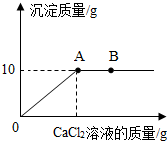 现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求
现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求(1)恰好反应时生成沉淀的质量为:10克
(2)B点溶液中的溶质为:NaCl、CaCl2
(3)恰好完全反应时所得溶液的溶质质量数.
分析 根据图中通过的数据可以判断生成沉淀的质量;
根据沉淀的质量可以计算碳酸钠的质量和生成的氯化钠的质量,进一步可以计算恰好完全反应时所得溶液的溶质质量数.
解答 解:(1)由图中数据可知,恰好反应时生成沉淀碳酸钙的质量是10g;
故填:10.
(2)B点溶液中的溶质包括氯化钠和过量的氯化钙,即B点溶液中的溶质为NaCl、CaCl2.
故填:NaCl、CaCl2.
(3)设碳酸钠的质量为x,生成氯化钠的质量为y,氯化钙的质量为z,
Na2CO3+CaCl2═CaCO3↓+2NaCl,
106 111 100 117
x z 10g y
$\frac{106}{x}$=$\frac{111}{z}$=$\frac{100}{10g}$=$\frac{117}{y}$,
x=10.6g,y=11.7g,z=11.1g,
恰好完全反应时氯化钙溶液的质量为:11.1g÷10%=111g,
恰好完全反应时所得溶液的溶质质量数为:$\frac{22.3g-10.6g+11.7g}{99g+111g-10g}$×100%=11.7%,
答:恰好完全反应时所得溶液的溶质质量数为11.7%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
6.下列物质不必密封保存的是( )
| A. | 生石灰 | B. | 石灰石 | C. | 浓盐酸 | D. | 浓硫酸 |
7.下列实验的基本操作正确的是( )
| A. |  浓硫酸的稀释 | B. |  称量一定质量的食盐 | ||
| C. |  过滤 | D. |  检查装置的气密性 |
1.下列实验操作中正确的是( )
| A. |  塞紧橡胶塞 | B. |  过滤 | C. |  测溶液PH | D. |  倾倒液体 |
5.下列关于一氧化碳和二氧化碳两种气体的叙述不正确的是( )
| A. | 二氧化碳的大量排放会造成温室效应 | |
| B. | 一氧化碳易与血红蛋白结合能使人中毒 | |
| C. | 一氧化碳和二氧化碳都能使澄清石灰水变浑浊 | |
| D. | 向种植蔬菜的大棚中补充适量的二氧化碳有利于蔬菜的生长 |
1.金属是一种非常重要的资源,在生产、生活中有着广泛的用途.
(1)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是硝酸银.
②说明Mg比Fe活泼的实验现象是与酸反应镁比铁剧烈
③说明Cu比Ag活泼的实验现象是铜丝表面有一层银白色物质生成.
(2)生铁是铁和碳的合金.为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入98g稀硫酸,恰好完全反应(杂质不参与反应也不溶于水).测得的实验数据如表;
请你完成有关计算:
(1)反应产生的氢气质量为多少
(2)稀硫酸中溶质的质量分数是多少?
(1)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是硝酸银.
②说明Mg比Fe活泼的实验现象是与酸反应镁比铁剧烈
③说明Cu比Ag活泼的实验现象是铜丝表面有一层银白色物质生成.
(2)生铁是铁和碳的合金.为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入98g稀硫酸,恰好完全反应(杂质不参与反应也不溶于水).测得的实验数据如表;
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 170.0g | 169.8g |
(1)反应产生的氢气质量为多少
(2)稀硫酸中溶质的质量分数是多少?