题目内容
1.金属是一种非常重要的资源,在生产、生活中有着广泛的用途.(1)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请回答下列问题:
①亮亮所用的另一种溶液是硝酸银.
②说明Mg比Fe活泼的实验现象是与酸反应镁比铁剧烈
③说明Cu比Ag活泼的实验现象是铜丝表面有一层银白色物质生成.
(2)生铁是铁和碳的合金.为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入98g稀硫酸,恰好完全反应(杂质不参与反应也不溶于水).测得的实验数据如表;
| 反应前 | 反应后 | |
| 烧杯及其中物质的质量 | 170.0g | 169.8g |
(1)反应产生的氢气质量为多少
(2)稀硫酸中溶质的质量分数是多少?
分析 (1)根据金属活动性顺序表及其应用分析,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;
(2)根据铁会与硫酸反应生成硫酸亚铁和氢气,反应后烧杯中减少的质量就是氢气的质量,然后结合化学方程式计算出参加反应的硫酸的质量,再计算质量分数.
解答 解:(1)①由金属活动性顺序表及其应用可知,运用稀盐酸首先可验证镁比铁活泼,镁、铁比铜、银活泼.因为稀盐酸和铁镁能反应生成氢气,而铜银与稀盐酸不反应不产生氢气,且镁比铁产生氢气的速度快.但不能验证铜和银的金属活动性.利用金属活动顺序表中前面的金属能把后面的金属从它的化合物的溶液中置换出来,可用硝酸银溶液来比较铜银的活动性;
②说明Mg比Fe活泼的实验现象是:镁与稀盐酸反应速度比铁与稀盐酸反应速度快;
③说明Cu比Ag活泼的实验现象是:铜丝放入硝酸银溶液中,铜丝的表面有银白的金属生成;
(2)根据质量守恒定律可知,生成氢气的质量为:170g-169.8gg=0.2g;
设参加反应的硫酸的质量为x,
Fe+H2SO4=FeSO4+H2↑
98 2
x 0.2g
$\frac{98}{x}$=$\frac{2}{0.2g}$
x=9.8g
所以稀硫酸中溶质的质量分数是:$\frac{9.8g}{98g}$×100%=10%.
故答案为:(1)①硝酸银溶液;
②与酸反应镁比铁剧烈;
③铜丝表面有一层银白色物质生成;
(2)0.2g,10%.
点评 该题难度适中,主要考查了对金属活动性顺序的灵活运用,及根据化学方程式进行有关的计算,培养学生应用知识的能力.

练习册系列答案
相关题目
9.逻辑推理是化学学习常用的思维方法,下列推理正确的是( )
| A. | 碱的溶液呈碱性,则碱性液体一定是碱的溶液 | |
| B. | 中和反应生成盐和水,则生成盐和水的反应一定是中和反应 | |
| C. | 单质中只含有一种元素,则只含有一种元素的纯净物一定是单质 | |
| D. | 碳酸盐与盐酸反应生成气体,则与盐酸反应生成气体的物质一定是碳酸盐 |
6.下列图象分别于选项中的操作相对应其中合理的是( )
| A. | 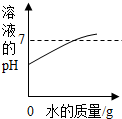 向一定量稀硫酸中滴加水 | |
| B. |  向一定量纯碱和烧碱的混合溶液中滴入盐酸 | |
| C. | 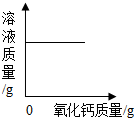 一定温度时向一定量饱和石灰水中加入氧化钙 | |
| D. | 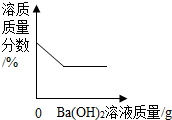 向稀硫酸中慢慢滴加Ba(OH)2溶液至过量 |
13.下列四个实验绝对不会造成环境污染的是( )

| A. | ①② | B. | ③④ | C. | ②③ | D. | ①④ |
10.有句谚语“每天一个苹果,医生远离我”,苹果主要能为人体提供的营养素是( )
| A. | 维生素 | B. | 油脂 | C. | 蛋白质 | D. | 糖类 |
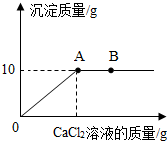 现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求
现有NaCl和Na2CO3混合物22.3克,加水完全溶解,形成99克溶液,往该溶液中逐滴加入10%的CaCl2溶液,产生沉淀的质量和所加CaCl2溶液的质量关系如图所示,求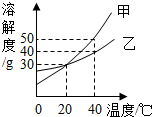 如图为甲、乙两种物质的溶解度曲线,请回答下列问题:
如图为甲、乙两种物质的溶解度曲线,请回答下列问题: