题目内容
2.城市污水井、排污管道经常发生中毒事故或因燃放炮竹引发的爆炸事故.某小组同学在专业人员帮助下收集气体样品对其成分进行探究.【查阅资料】
I 城市污水井、排污管道中的有机物质发酵会产生CO、CO2、H2S、CH4等气体.
Ⅱ硫化氢(H2S)有剧毒,溶于水形成氢硫酸,实验室中除去H2S的方法是将其通入硫酸铜溶液中,形成黑色的硫化铜,化学方程式为CuSO4+H2S═CuS↓+H2SO4.
Ⅲ等体积均为10%的邻苯三酚溶液与氢氧化钠溶液混合时可以快速除去氧气,且溶液颜色逐渐变深.
【进行实验】小组同学设计了下图所示的装置并进行探究.

通入气体样品前先通入N2排出各装置中的空气.
实验现象记录与分析:
| 实验现象 | 结论与化学方程式 |
| A中出现黑色固体;B中澄清石灰水变浑浊;D中溶液逐渐变为墨绿色;F中烧杯内壁出现无色液滴. | B中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;装置E中药品的作用是除去气体中混有的水蒸气;收集的气体样品中一定含有H2S、CO2、CH4、O2. |
(1)该实验中无法确定的气体是CO,确定是否含有该气体中的方法是:收集燃烧产物,将燃烧产物依次通过盛有浓硫酸和氢氧化钠溶液的装置,分别称量吸收燃烧产物前、吸收燃烧产物后装置的质量,通过计算、分析得出结论.
(2)实验中若检验H2S后就检验氧气,是否能得到实验结论、理由是不能,因为除去氧气的药品中含有NaOH,除去氧气的同时也将CO2除去了.
分析 【进行实验】根据二氧化碳会与氢氧化钙反应生成碳酸钙沉淀,浓硫酸具有吸水性,A中出现黑色固体;B中澄清石灰水变浑浊;D中溶液逐渐变为墨绿色;F中烧杯内壁出现无色液滴进行分析;
【实验反思】(1)根据一氧化碳具有可燃性,二氧化碳会与氢氧化钠反应进行分析;
(2)根据除去氧气的药品中含有NaOH,除去氧气的同时也会将CO2除去进行分析.
解答 解:【进行实验】二氧化碳会与氢氧化钙反应生成碳酸钙沉淀,浓硫酸具有吸水性,A中出现黑色固体,说明混合气中有硫化氢;B中澄清石灰水变浑浊,说明混合气中含有二氧化碳;D中溶液逐渐变为墨绿色,说明混合气中含有氧气;F中烧杯内壁出现无色液滴,说明混合气中含有甲烷,所以
| 实验现象 | 结论与化学方程式 |
| A中出现黑色固体;B中澄清石灰水变浑浊;D中溶液逐渐变为墨绿色;F中烧杯内壁出现无色液滴. | B中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;装置E中药品的作用是除去气体中混有的水蒸气;收集的气体样品中一定含有H2S、CO2、CH4、O2. |
(2)除去氧气的药品中含有NaOH,除去氧气的同时也会将CO2除去,所以检验H2S后就检验氧气,不能得到实验结论.
故答案为:【进行实验】CO2+Ca(OH)2═CaCO3↓+H2O,除去气体中混有的水蒸气,H2S、CO2、CH4、O2;
| 实验现象 | 结论与化学方程式 |
| CO2+Ca(OH)2═CaCO3↓+H2O;除去气体中混有的水蒸气;H2S、CO2、CH4、O2. |
(2)不能,因为除去氧气的药品中含有NaOH,除去氧气的同时也将CO2除去了.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
12.对下列相关事实用微观粒子的知识解释正确的是( )
| 选项 | 事 实 | 解释 |
| A | 氯化钠固体不导电 | 氯化钠固体中没有离子 |
| B | 有机物数目种类异常庞大 | 原子的排列方式不同,性质不同 |
| C | 水烧开后水壶盖容易被顶起 | 温度升高分子运动加快,体积变大 |
| D | 水结冰后不能流动 | 0℃以下,水分子不再运动 |
| A. | A | B. | B | C. | C | D. | D |
13.如图分别是铝元素、氯元素的原子结构示意图.下列叙述正确的是( )
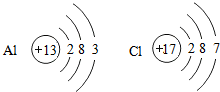

| A. | 铝原子第一电子层有3个电子 | B. | 氯原子核内有17个质子 | ||
| C. | 氯原子在化学反应中容易失去电子 | D. | 铝原子核带13个单位负电荷 |
7.维生素C(化学式为C6H8O6)是人体不可缺少的营养物质.下列关于维生素C的叙述正确的是( )
| A. | 是氧化物 | |
| B. | 氧元素的质量分数计算式为$\frac{6}{176}$×100% | |
| C. | 每个分子中含有20个原子 | |
| D. | 碳、氢、氧三种元素的质量比3:4:3 |

 某固体物可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验.
某固体物可能由Na2SO4、NaCl、Na2CO3、KNO3中的一种或几种组成,现进行如下实验.