题目内容
13.如图分别是铝元素、氯元素的原子结构示意图.下列叙述正确的是( )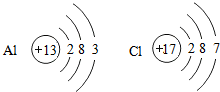
| A. | 铝原子第一电子层有3个电子 | B. | 氯原子核内有17个质子 | ||
| C. | 氯原子在化学反应中容易失去电子 | D. | 铝原子核带13个单位负电荷 |
分析 原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
解答 解:A、由铝原子的结构示意图,铝原子第一电子层有2个电子,故选项说法错误.
B、由氯原子的结构示意图,圆圈内的数字是17,该元素原子核内有17个质子,故选项说法正确.
C、由氯原子的结构示意图,最外层电子数是7,在化学反应中易得到1个电子而形成阴离子,故选项说法错误.
D、由铝原子的结构示意图,圆圈内的数字是13,该元素原子核内有13个质子,质子带正电,中子不带电,则铝原子核带13个单位正电荷,故选项说法错误.
故选:B.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.

练习册系列答案
相关题目
3.下列各组物质,用一种试剂一次就能鉴别开来的是( )
| A. | 炭粉、氧化铜粉末、铁粉 | B. | 氢气、二氧化碳、氮气 | ||
| C. | 氯化钾、氯化铵、硝酸铵 | D. | 氢氧化钾、熟石灰、烧碱 |
4.化学小组的同学分析某无色透明的溶液中含有三种溶质,其中可能正确的是( )
| A. | NaCl、KNO3.(NH4)2SO4 | B. | HC1、AgNO3.Na2SO4 | ||
| C. | KMnO4、CuCl2、Fe2(SO4)3 | D. | H2SO4、K2CO3、NaOH |
8. 甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示.下列叙述正确的是( )
 甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙两种物质(均不含结晶水)的溶解度曲线如图所示.下列叙述正确的是( )| A. | t2℃时,50g甲的饱和溶液中含有15g甲 | |
| B. | t1℃时,甲、乙两种物质的饱和溶液溶质的质量分数一定相等 | |
| C. | 从含有少量甲的乙的饱和溶液中得到较多的乙晶体,可采用冷却热饱和溶液的方法 | |
| D. | 分别将t2℃时,甲的饱和溶液、乙的饱和溶液降温至t1℃,若析出甲的质量大于析出乙的质量,则t2℃时甲、乙两种饱和溶液中溶剂的质量不可能相等 |
5.下列实验操作中,不正确的是( )
| A. | 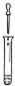 滴加液体药品 | B. | 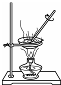 蒸发食盐水 | C. | 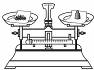 称量固体 | D. | 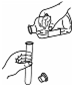 倾倒液体 |
2.城市污水井、排污管道经常发生中毒事故或因燃放炮竹引发的爆炸事故.某小组同学在专业人员帮助下收集气体样品对其成分进行探究.
【查阅资料】
I 城市污水井、排污管道中的有机物质发酵会产生CO、CO2、H2S、CH4等气体.
Ⅱ硫化氢(H2S)有剧毒,溶于水形成氢硫酸,实验室中除去H2S的方法是将其通入硫酸铜溶液中,形成黑色的硫化铜,化学方程式为CuSO4+H2S═CuS↓+H2SO4.
Ⅲ等体积均为10%的邻苯三酚溶液与氢氧化钠溶液混合时可以快速除去氧气,且溶液颜色逐渐变深.
【进行实验】小组同学设计了下图所示的装置并进行探究.

通入气体样品前先通入N2排出各装置中的空气.
实验现象记录与分析:
【实验反思】
(1)该实验中无法确定的气体是CO,确定是否含有该气体中的方法是:收集燃烧产物,将燃烧产物依次通过盛有浓硫酸和氢氧化钠溶液的装置,分别称量吸收燃烧产物前、吸收燃烧产物后装置的质量,通过计算、分析得出结论.
(2)实验中若检验H2S后就检验氧气,是否能得到实验结论、理由是不能,因为除去氧气的药品中含有NaOH,除去氧气的同时也将CO2除去了.
【查阅资料】
I 城市污水井、排污管道中的有机物质发酵会产生CO、CO2、H2S、CH4等气体.
Ⅱ硫化氢(H2S)有剧毒,溶于水形成氢硫酸,实验室中除去H2S的方法是将其通入硫酸铜溶液中,形成黑色的硫化铜,化学方程式为CuSO4+H2S═CuS↓+H2SO4.
Ⅲ等体积均为10%的邻苯三酚溶液与氢氧化钠溶液混合时可以快速除去氧气,且溶液颜色逐渐变深.
【进行实验】小组同学设计了下图所示的装置并进行探究.

通入气体样品前先通入N2排出各装置中的空气.
实验现象记录与分析:
| 实验现象 | 结论与化学方程式 |
| A中出现黑色固体;B中澄清石灰水变浑浊;D中溶液逐渐变为墨绿色;F中烧杯内壁出现无色液滴. | B中发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O;装置E中药品的作用是除去气体中混有的水蒸气;收集的气体样品中一定含有H2S、CO2、CH4、O2. |
(1)该实验中无法确定的气体是CO,确定是否含有该气体中的方法是:收集燃烧产物,将燃烧产物依次通过盛有浓硫酸和氢氧化钠溶液的装置,分别称量吸收燃烧产物前、吸收燃烧产物后装置的质量,通过计算、分析得出结论.
(2)实验中若检验H2S后就检验氧气,是否能得到实验结论、理由是不能,因为除去氧气的药品中含有NaOH,除去氧气的同时也将CO2除去了.
3.实验室中用过氧化氢、氯酸钾、高锰酸钾等都可以制取氧气,其原因是( )
| A. | 都属于盐 | B. | 都含有氧气 | C. | 都含有氧元素 | D. | 都含有氧气分子 |