题目内容
5.完成下列变化的化学方程式,并按要求填空.(1)天然气燃烧:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O,该反应放热(填写“放热”或“吸热”);
(2)稀硫酸除铁锈:Fe2O3+6HCl═2FeCl3+3H2O,溶液由无色变为黄色;
(3)工业上用赤铁矿炼铁的原理:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,冶炼生铁的主要设备是高炉;
(4)若不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的水冲洗,然后涂上3%~5%的NaHCO3溶液:2NaHCO3+H2SO4═Na2SO4+H2O+2CO2↑;该反应的基本类型是复分解反应;
(5)少量硫酸铵固体与熟石灰混合研磨:(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;检验该气体可用湿润的红色石蕊试纸.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)天然气的主要成分是甲烷,甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;该反应属于放热反应.
(2)铁锈的主要成分是氧化铁,与盐酸反应生成氯化铁和水,反应的化学方程式是:Fe2O3+6HCl═2FeCl3+3H2O;溶液由无色变为黄色.
(3)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;冶炼生铁的主要设备是高炉.
(4)NaHCO3溶液与稀硫酸反应生成硫酸、水和二氧化碳,反应的化学方程式为2NaHCO3+H2SO4═Na2SO4+H2O+2CO2↑;该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应.
(5)硫酸铵固体与熟石灰混合研磨生成硫酸钙、水和二氧化碳,反应的化学方程式是为:(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;生成的氨气可用湿润的红色石蕊试纸检验,若变蓝,说明是氨气.
故答案为:(1)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;放热;
(2)Fe2O3+6HCl═2FeCl3+3H2O;黄色;
(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;高炉;
(4)2NaHCO3+H2SO4═Na2SO4+H2O+2CO2↑;复分解反应;
(5)(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;湿润的红色石蕊.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案| A. | 果汁中含有有机物 | B. | 用炉具清洁剂刷洗坐便器 | ||
| C. | 用浓硫酸干燥氨气 | D. | 溶液都能导电 |
【查阅资料】变色硅胶吸水后由蓝色变为红色.无水醋酸是一种酸,常温下为无色液体.
【实验探究】
| 实 验 操 作 | 现 象 | 结 论 |
| (1)在氢氧化钠溶液的烧杯中,滴加2-3滴酚酞试液,用胶头滴管逐滴滴加盐酸,边滴边搅拌. | 溶液刚好由红色变成无色. | 反应中碱的特性消失了(溶液不呈碱性) |
| (2)取实验1 所得少量溶液于试管中,向其中加入一滴氢氧化钠溶液. | 溶液由无色变成红色 | 反应中酸的特性消失了. |
(3)取变色硅胶、无水醋酸和氢氧化钠固体进行如下图所示的三个实验.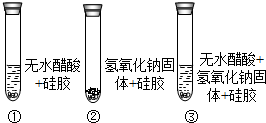 | ①②中硅胶不变红,③中硅胶变红 | 反应生成了水. |
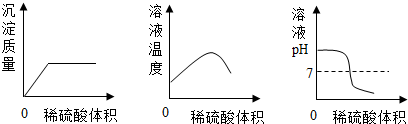
【实验拓展】用传感技术能更准确方便地探究反应的实质.如图是用常见的传感器进行的氢氧化钡溶液中滴加稀硫酸的实验结果,其中能说明中和反应实质的是C(填序号).(注:Ba(OH)2+H2SO4=BaSO4↓+2H2O)
 化学是在原子、分子、离子水平上研究物质及其变化的科学.
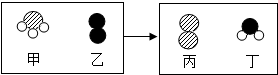
化学是在原子、分子、离子水平上研究物质及其变化的科学.(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.下列说法正确的是BE (填序号)
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-、CO32-.
| A. | 3O-3个氧元素 | B. | $\stackrel{+3}{Fe}$-1个铁离子 | ||
| C. | O3-3个氧原子 | D. | SO3-1个三氧化硫分子 |
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是A (填“A”或“B”);

(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是20℃~30℃;
(3)某兴趣小组做了以下实验:

上述实验过程中得到的溶液一定属于不饱和溶液的是①③④ (填数字序号).
将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体59.1 g,所得滤液中KNO3的溶质质量分数为17.3%.(计算结果保留小数点后1位,不考虑实验过程中水的蒸发)
| A. | 木炭 | B. | 铁丝 | C. | 硫粉 | D. | 红磷 |