题目内容
17.KNO3和NaCl在不同温度时的溶解度如下表:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
(1)依据上表数据,绘制出KNO3和NaCl的溶解度曲线如图,图中能表示KNO3溶解度曲线的是A (填“A”或“B”);

(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解度,则温度的取值范围是20℃~30℃;
(3)某兴趣小组做了以下实验:

上述实验过程中得到的溶液一定属于不饱和溶液的是①③④ (填数字序号).
将⑤继续冷却至10℃,过滤,共可回收得到KNO3固体59.1 g,所得滤液中KNO3的溶质质量分数为17.3%.(计算结果保留小数点后1位,不考虑实验过程中水的蒸发)
分析 (1)根据表中两物质的溶解度随温度变化的情况分析解决;
(2)根据表中两物质的溶解度随温度变化的情况分析解决;
(3)根据20℃、50℃、10℃硝酸钾的溶解度进行解答.
解答 解:(1)从表中数据可以看出氯化钠的溶解度随温度改变大小变化不明显,而硝酸钾变化很明显,所以表示KNO3溶解度曲线的是A图象,
(2)由表中数据分析可知,KNO3和NaCl在某一温度时具有相同的溶解度,分析表中数据20℃~30℃的温度范围适合;
(3)20℃硝酸钾的溶解度为31.6g,所以100g水中加入25g硝酸钾,全部溶解,①溶液为不饱和溶液;50℃时硝酸钾的溶解度是85.5g,原溶液中已有硝酸钾80g,所以③④溶液为不饱和溶液;将⑤继续冷却至10℃,此时硝酸钾的溶解度为20.9g,过滤,共可回收得到KNO3固体:80g-20.9g=59.1g;所得滤液中KNO3的溶质质量分数为:$\frac{20.9g}{100g+20.9g}$×100%≈17.3%.
故答案为:(1)A;
(2)20℃~30℃;
(3)①③④;59.1;17.3%.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线中看出的①同一溶质在不同温度下的溶解度;②同一温度下,不同溶质的溶解度;③温度对不同物质的溶解度影响不同等都是解决此类题的关键.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
8.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在氯化钠溶液中:Fe3+、Ca2+、NO${\;}_{3}^{-}$ | |
| B. | 在稀盐酸中:Ba2+、Zn2+、CO${\;}_{3}^{2-}$ | |
| C. | 在氢氧化钠溶液中:H+、Mg2+、Cl- | |
| D. | 在硫酸铵溶液中:Na+、K+、OH- |
12.酸、碱、盐在工农业生产和日常生活中的广泛应用,促进了人类文明的进步和社会的可持续发展.下列有关酸、碱、盐的生产或应用的说法不合理的是( )
| A. | 将草木灰(含K2CO3)与氯化铵混合施用 | |
| B. | 纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 | |
| C. | 用石灰乳粉刷墙壁 | |
| D. | 用稀硫酸“酸洗”除去钢铁表面的铁锈 |
2. 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
 某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的溶质质量分数相等的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )| A. | 金属活动性由强到弱:X、Z、Y | B. | 金属活动性由强到弱:X、Y、Z | ||
| C. | X、Y、Z依次可能是Mg、Zn、Fe | D. | 相对原子质量的大小:Y>Z>X |
9.某同学用下列方法清洗试管或烧杯,其中不正确的是( )
| A. | 用水清洗装过硫酸铜溶液的试管 | |
| B. | 用洗洁精清洗盛过植物油的烧杯 | |
| C. | 用酒精清洗试管内壁残留的固体碘 | |
| D. | 用稀盐酸浸泡用足量木炭还原氧化铜后试管内壁留下的红色物质 |
6.我国纪念2015年“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.下列有关水的说法中正确的是( )
| A. | 电解水实验中,负极与正极产生的气体质量比约为2:1 | |
| B. | 可以用肥皂水鉴别软水和硬水 | |
| C. | 加入明矾,可以将硬水转化为软水 | |
| D. | 经过沉淀、过滤并加活性炭吸附后得到的水,可以直接饮用 |
7.下列各组物质中的杂质除去方案合理的是A
| 选项 | 杂质 | 除杂质所用试剂或方法 |
| A.H2 | HCl气体 | 先通过NaOH溶液,再通过浓硫酸 |
| B.NaOH | Ba(OH)2溶液 | 先加入CuSO4溶液、过滤 |
| C.CO | CO2气体 | 通过灼热的CuO |
| D CuCl2 | Cu(OH)2 | 加入足量稀盐酸,再进行蒸发 |
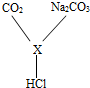 请你用所学的化学原理解释.
请你用所学的化学原理解释.