题目内容
16.某同学对于书本48页“酸和碱反应的结果是酸和碱各自的特性都消失,生成盐和水”的描述产生了兴趣,设计以下实验进行验证探究.【查阅资料】变色硅胶吸水后由蓝色变为红色.无水醋酸是一种酸,常温下为无色液体.
【实验探究】
| 实 验 操 作 | 现 象 | 结 论 |
| (1)在氢氧化钠溶液的烧杯中,滴加2-3滴酚酞试液,用胶头滴管逐滴滴加盐酸,边滴边搅拌. | 溶液刚好由红色变成无色. | 反应中碱的特性消失了(溶液不呈碱性) |
| (2)取实验1 所得少量溶液于试管中,向其中加入一滴氢氧化钠溶液. | 溶液由无色变成红色 | 反应中酸的特性消失了. |
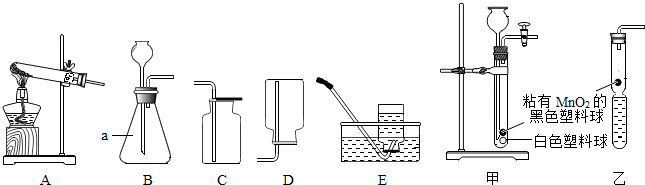
(3)取变色硅胶、无水醋酸和氢氧化钠固体进行如下图所示的三个实验.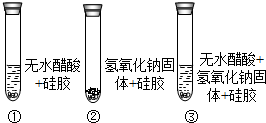 | ①②中硅胶不变红,③中硅胶变红 | 反应生成了水. |
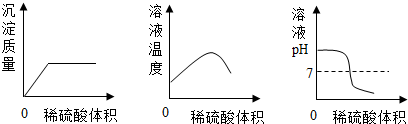
【实验拓展】用传感技术能更准确方便地探究反应的实质.如图是用常见的传感器进行的氢氧化钡溶液中滴加稀硫酸的实验结果,其中能说明中和反应实质的是C(填序号).(注:Ba(OH)2+H2SO4=BaSO4↓+2H2O)
分析 【探究活动】根据酚酞在酸、碱溶液中的颜色的变化分析;根据硅胶的颜色的变化分析反应是否有有水生成;
【实验结论】根据酸中的氢离子和碱中的氢氧根离子结合生成水分子解答;
【实验拓展】观察图象,根据变化的趋势.分析溶液的酸碱性变化,能量的变化.
解答 解:
【探究活动】(1)无色酚酞试液在氢氧化钠溶液中显红色,滴入了稀盐酸变成了无色,说明了盐酸与氢氧化钠发生了反应;
(2)取实验1 所得少量溶液于试管中,向其中加入一滴氢氧化钠溶液.溶液由无色变成红色,反应中酸的特性消失了.
(3)通过实验①、②的实验现象的对比证明了无水醋酸和氢氧化钠不含有水,不能使硅胶变色,由试验③硅胶的变色说明了中和反应有水生成.
【实验结论】从微观本质上看,中和反应的实质是:酸中的氢离子和碱中的氢氧根离子结合生成水分子,H++OH-═H2O;
【实验拓展】由pH曲线随着滴入的氢氧化钠的增多,pH增大,当t1时pH=7,说明了酸与碱发生了中和反应;由温度的变化曲线可以看出,曲线逐渐上升,说明了中和反应是放热反应.
答案:
【实验探究】(1)反应中碱的特性消失了(溶液不呈碱性)
(2)溶液由无色变成红色
(3)①②中硅胶不变红,③中硅胶变红
【实验结论】H++OH-═H2O
【实验拓展】C
点评 本题属于实验探究题,综合性较强,既有试验探究,又有实验数据图象的分析.只有综合掌握了基础知识才能较好的完成本类练习题.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.下列操作正确的是( )
| A. | 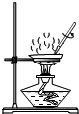 蒸发溶剂 | B. |  稀释浓硫酸 | ||
| C. | 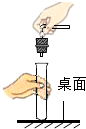 在桌面上塞上橡皮塞 | D. | 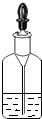 滴瓶上的滴管清洗后放回 |
4.下列物质不属于氮肥的是( )
| A. | NH4NO3 | B. | NH4HCO3 | C. | K2SO4 | D. | CO(NH2)2 |
1.地壳中含量最多的金属元素所对应的氧化物是( )
| A. | SiO2 | B. | CaO | C. | Al2O3 | D. | Fe2O3 |
8.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在氯化钠溶液中:Fe3+、Ca2+、NO${\;}_{3}^{-}$ | |
| B. | 在稀盐酸中:Ba2+、Zn2+、CO${\;}_{3}^{2-}$ | |
| C. | 在氢氧化钠溶液中:H+、Mg2+、Cl- | |
| D. | 在硫酸铵溶液中:Na+、K+、OH- |
6.我国纪念2015年“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.下列有关水的说法中正确的是( )
| A. | 电解水实验中,负极与正极产生的气体质量比约为2:1 | |
| B. | 可以用肥皂水鉴别软水和硬水 | |
| C. | 加入明矾,可以将硬水转化为软水 | |
| D. | 经过沉淀、过滤并加活性炭吸附后得到的水,可以直接饮用 |
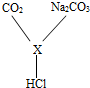 请你用所学的化学原理解释.
请你用所学的化学原理解释.