题目内容
10.实验室测定某铝土矿中铝元素的质量分数,取13.5g含杂质的铝土矿(杂质不溶于水也不与酸反应)加入到200g稀盐酸中,恰好完全反应,过滤得滤液210.2g,则该铝土矿中铝元素的质量分数为( )| A. | 75.6% | B. | 40% | C. | 50% | D. | 60% |
分析 根据反应前后过滤得到的滤液的质量和原物质的质量差为杂质,可得氧化铝的质量,进而求算出铝元素的质量,最后求算铝元素在矿石中的质量分数.
解答 解:杂质的质量为13.5g+200g-210.2g=3.3g.
则氧化铝的质量为13.5g-3.3g=10.2g
则氧化铝中铝元素的质量为10.2g×$\frac{27×2}{27×2+16×3}$×100%=5.4g
则铝元素在矿石中的质量分数为$\frac{5.4g}{13.5g}$×100%=40%.
故选:B.
点评 本题由于不生成气体,所以溶液和反应前的质量差就是杂质的质量,进而求算出氧化铝的质量,而无需根据化学方程式进行计算.

练习册系列答案
相关题目
20.将6.8g含杂质的锌粒,加入到盛有50.0g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6g,求生成氢气的质量( )g.(化学方程式:Zn+H2SO4═ZnSO4+H2↑)
| A. | 0.1 | B. | 0.2 | C. | 0.3 | D. | 0.4 |
5.关注健康,预防疾病.下列叙述正确的是( )
| A. | 人体通过食物获得的蛋白质在胃肠道内与氧气发生反应,生成氨基酸 | |
| B. | 维生素有20多种,在人体内都不能合成,只能从食物中摄取 | |
| C. | 每克油脂在人体内完全氧化,放出的能量比糖类多,是重要的供能物质 | |
| D. | 铁、锌、锡、碘、氟都是人体所需的微量元素 |
4.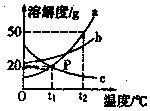 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,根据图中已给信息判断下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,根据图中已给信息判断下列说法错误的是( )
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,根据图中已给信息判断下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点,根据图中已给信息判断下列说法错误的是( )| A. | P点的含义是t1℃时,a与c的溶解度相等 | |
| B. | t2℃时,a、b、c三种物质溶解度由小到大顺序为c b a | |
| C. | 将t2℃时a、b两种饱和溶液降温到t1℃时,析出晶体的质量a大于b | |
| D. | 将t1℃时,a、c两种物质饱和溶液的温度升高到t2℃时,所得两种溶液的质量分数a大于c |
5.在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如表:
下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 56 | 18 | 2 | 0 |
| 反应后的质量(g) | 10 | 0 | 2 | X |
| A. | x为64 | B. | 参加反应的乙的质量为18g | ||
| C. | 参加反应的甲物质的质量为46g | D. | 丙物质一定作催化剂 |
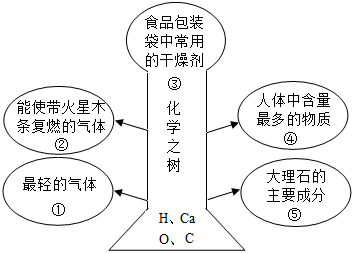 学习化学一定要正确使用化学语言,按要求完成各题.
学习化学一定要正确使用化学语言,按要求完成各题.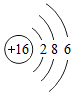 和氧原子
和氧原子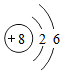 化学性质相似的原因为最外层电子数相同.
化学性质相似的原因为最外层电子数相同.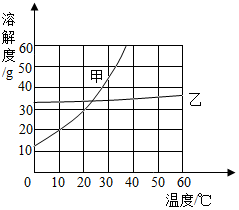 分析甲、乙两种固体的溶解度曲线,回答问题.
分析甲、乙两种固体的溶解度曲线,回答问题.