题目内容
16.根据下列实验装置,回答有关问题: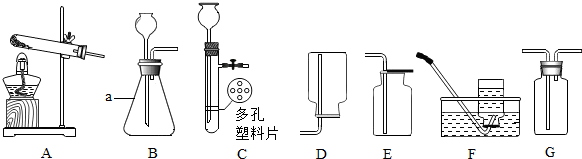
(1)仪器a的名称是锥形瓶.
(2)实验室用氯酸钾和二氧化锰的混合物制取并收集较纯净的氧气,应该选择的装置是A、F(填序号),反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)小红用大理石和浓度较大的盐酸制取CO2,为了得到纯净、干燥的CO2,在B装置后面连续连接了两个G装置再连接E装置进行收集,小红设计第一个G装置的作用是除去氯化氢气体,第二个G装置中盛放的试剂是浓硫酸.小明认为用装置C代替气体发生装置B更好,理由是能控制反应的发生和停止.
分析 锥形瓶是常用的反应容器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.小红设计第一个G装置的作用是除去氯化氢气体;第二个G装置中盛放的试剂是浓硫酸,起干燥作用;小明认为用装置C代替气体发生装置B更好,理由是能控制反应的发生和停止.
解答 解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,排水法收集的氧气比较纯净;故答案为:A、F;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)小红设计第一个G装置的作用是除去氯化氢气体;第二个G装置中盛放的试剂是浓硫酸,起干燥作用;小明认为用装置C代替气体发生装置B更好,理由是能控制反应的发生和停止;故答案为:除去氯化氢气体;浓硫酸;能控制反应的发生和停止;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、气体的干燥和除杂等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.下列各组物质按单质、化合物、混合物的顺序排列的是( )
| A. | 木炭、氧化铜、空气 | B. | 氮气、过氧化氢溶液、氯酸钾 | ||
| C. | 矿泉水、水银、牛奶 | D. | 金刚石、干冰、石灰石 |
7.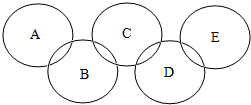 如图所示,A、B、C、D、E分别属于单质、氧化物、酸、碱、盐五种不同类别的物质,若两环相连表示两种物质之间能相互发生反应,则下列说法正确的是( )
如图所示,A、B、C、D、E分别属于单质、氧化物、酸、碱、盐五种不同类别的物质,若两环相连表示两种物质之间能相互发生反应,则下列说法正确的是( )
 如图所示,A、B、C、D、E分别属于单质、氧化物、酸、碱、盐五种不同类别的物质,若两环相连表示两种物质之间能相互发生反应,则下列说法正确的是( )
如图所示,A、B、C、D、E分别属于单质、氧化物、酸、碱、盐五种不同类别的物质,若两环相连表示两种物质之间能相互发生反应,则下列说法正确的是( )| A. | 若物质A为单质,则物质B只能是氧化物 | |
| B. | 五种物质A、B、C、D、E依次可为CO2、Ca(OH)2、Na2CO3、HCl、Cu | |
| C. | 若物质C为稀盐酸,则物质C与E一定不能发生反应 | |
| D. | 物质C一定不能是氧化物 |
11.除去下列物质中的少量杂质,所用试剂及操作方法如下所示,其中正确的是( )
| 选项 | 物质 | 杂质 | 所用试剂及操作方法 |
| A | CO2 | CO | 通入足量的氧气,点燃 |
| B | NaNO3溶液 | Na2CO3溶液 | 加入适量的CaCl2溶液,过滤 |
| C | CuSO4溶液 | H2SO4 | 加入过量的CuO粉末,过滤 |
| D | NaCl溶液 | Fe2(SO4)3溶液 | 加入过量的Ba(OH)2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.鉴别下列物质所用的方法或试剂,错误的是( )
| A. | 硬水和软水--肥皂水 | B. | 黄金和黄铜--比较颜色 | ||
| C. | 碳酸钠和氯化钠--稀盐酸 | D. | 羊毛和尼龙--灼烧法 |
6.造成煤气中毒的物质是( )
| A. | CO | B. | CH4 | C. | CO2 | D. | SO2 |

