题目内容
4.A、B、C、D、E、F、G、H、I、J、K都是九年级化学常见的物质,H的水溶液呈浅绿色,I为红色固体,它们之间的转化关系如图所示(反应条件已省略).
写化学方程式:C+A→CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.F+G→Fe+CuSO4═FeSO4+CuC→JCa(OH)2+CO2=CaCO3↓+H2O.H→KFeSO4+Ba(NO3)2=BaSO4↓+Fe(NO3)2.
分析 根据题干提供的信息进行分析解答,H的水溶液呈浅绿色,且能与硝酸钡反应产生白色沉淀,故H是硫酸亚铁溶液,K是硫酸钡;C能与澄清的石灰水反应产生白色沉淀J,故C是二氧化碳,J是碳酸钙;I为红色固体,F能与G反应生成硫酸亚铁和I,故I是铜,G是硫酸铜,F是铁;D和E能反应生成二氧化碳和铁,故可能是一氧化碳还原氧化铁的反应,A能与B反应生成一氧化碳,A能与B反应生成二氧化碳,二氧化碳能与碳反应生成一氧化碳,故A是碳,B是氧气,据此解答.
解答 解:H的水溶液呈浅绿色,且能与硝酸钡反应产生白色沉淀,故H是硫酸亚铁溶液,K是硫酸钡;C能与澄清的石灰水反应产生白色沉淀J,故C是二氧化碳,J是碳酸钙;I为红色固体,F能与G反应生成硫酸亚铁和I,故I是铜,G是硫酸铜,F是铁;D和E能反应生成二氧化碳和铁,故可能是一氧化碳还原氧化铁的反应,A能与B反应生成一氧化碳,A能与B反应生成二氧化碳,二氧化碳能与碳反应生成一氧化碳,故A是碳,B是氧气,带入框图,推断合理;
C是二氧化碳,A是IT按,碳与二氧化碳高温反应生成一氧化碳,故填:CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;
F是铁,G是硫酸铜溶液,铁能与硫酸铜反应生成硫酸亚铁和铜,故填:Fe+CuSO4═FeSO4+Cu;
C是二氧化碳,J是碳酸钙,二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,故填:Ca(OH)2+CO2=CaCO3↓+H2O;
H是硫酸亚铁,K是硫酸钡,硫酸亚铁和硝酸钡反应生成硫酸钡沉淀和硝酸亚铁,故填:FeSO4+Ba(NO3)2=BaSO4↓+Fe(NO3)2.
点评 这类题的解题方法或思路是:首先,分析好题意,既关注明显信息,又要挖掘出有用的隐含信息;然后,根据所学的掌握的基础知识,抓住关键信息,寻找突破口(即物质的特性或反应时的特殊现象等),细心地全面地思考、推断即可.

| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 氯酸钾和氯化钾 | 取样,加适量二氧化锰并加热 |
| B | 二氧化碳和一氧化碳 | 通入石蕊溶液,观察溶液是否变红 |
| C | 稀盐酸和稀硫酸 | 加镁条,观察是否有气泡 |
| D | 氮肥和磷肥 | 观察外观,呈灰白色的为磷肥 |
| A. | A | B. | B | C. | C | D. | D |
【提出问题】久置氢氧化钠固体的成分是什么?
【猜想与假设】
猜想Ⅰ:全部是NaOH;猜想Ⅱ:全部是Na2CO3;猜想Ⅲ:NaOH、Na2CO3.
【实验与探究】
(1)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 实验过程中始终没有气泡产生. | 则证明猜想Ⅰ成立. |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液. | 实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立. |
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性,能使酚酞变红,因此他认为该方案的操作步骤中应该改进的是继续滴加氯化钡溶液至过量,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
(3)实验小组的同学展开讨论,又提出了一个定量实验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立.实验如下:准确称取m克固体样品于试管中,加蒸馏水完全溶解,然后滴加足量氯化钡溶液,充分反应后过滤、洗涤、干燥称得沉淀的质量为n克,若猜想Ⅲ成立,则m与n的关系式为$\frac{106}{197}$n<m.
【反思与交流】久置的固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
| A. | 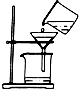 过滤 | B. | 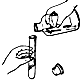 液体的倾倒 | C. |  闻气体气味 | D. | 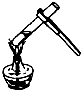 加热液体 |
| A. | “真金不怕火炼”是说黄金熔点很高 | |
| B. | “百炼成钢”与“只要功夫深铁杵磨成针”蕴含的化学原理相同 | |
| C. | “釜底抽薪”是一种灭火方法,其灭火的原理是清除可燃物 | |
| D. | “众人拾柴火焰高”是指可燃物越多,其着火点就越低,约容易燃烧 |
| A. | 氧气在低温、高压的条件下可以转化为液体或固体 | |
| B. | 氧气是植物光合作用的重要原料 | |
| C. | 氧气的化学性质比较活泼,是可燃物 | |
| D. | 氧气是可燃物燃烧的催化剂 |
| A. | NaClO | B. | NaCl | C. | NaCl2 | D. | Na |