题目内容
20.下面是关于物质分割的描述,其中分割到分子的是( )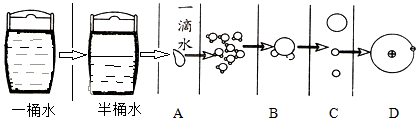
| A. | A | B. | B | C. | C | D. | D |
分析 根据分子是由原子构成的来分析解答.
解答 解:分子是由原子构成的.对分子进行分割也就是将每个水分子分成了2个氢原子和1个氧原子,观察图示可知,C选项符合题意.
故选C.
点评 本题考查了分子的构成,认真观察图示信息是解题的关键.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
15.根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:
(1)既能用D排水法,又能用C向上排空气法收集的气体是O2.
(2)用如图所示E盛满水的集气瓶收集CH4,气体应从b端进入.
(3)采用A装置制取气体比B装置制取气体,它的优点是可以随时添加液体药品,可以控制反应的速度

| 空气 | NH3 | CH4 | HCl | O2 | |
| 密度/g•L-1 | 1.293 | 0.771 | 0.717 | 1.629 | 1.43 |
| 溶解性 | ---- | 极易溶 | 难溶 | 极易溶 | 难溶 |
(2)用如图所示E盛满水的集气瓶收集CH4,气体应从b端进入.
(3)采用A装置制取气体比B装置制取气体,它的优点是可以随时添加液体药品,可以控制反应的速度

8.生命的孕育和维系需要水,科学研究离不开水.请你完成下列探究.
探究一:用水作溶剂.在盛有5ml水和5ml汽油的两只试管中各加入1~2小粒高锰酸钾,可观察到的现象是高锰酸钾溶于水形成紫红色溶液,而高锰酸钾难溶于汽油,结论:同一种物质在不同溶剂中的溶解性不同.
探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容.
探究三:溶质在水中的溶解与结晶.
【查阅资料】?20℃时,五种物质的溶解度如下表.
?相同温度下,不同溶质同时溶解在同一溶剂中,溶解度不变.
【提出问题】20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃).析出的晶体是什么?
【设计实验】设计方案,并进行实验.
(1)取少量晶体与熟石灰粉末混合、研磨,无明显现象.实验目的是证明晶体不是氯化铵.
(2)取少量晶体于试管中,加入盐酸,现象为有无色气体产生.
【实验结论】(3)析出的晶体是NaHCO3,晶体的质量为7.2g.
【实验拓展】(4)析出晶体的原因是NaCl和NH4HCO3溶于水未达饱和,所以不能以晶体析出,它们在水中解离出Na+、Cl-、NH4+、HCO3-,阴阳离子运动结合成NaHCO3和NH4Cl,由于NH4Cl溶解度较大,未达饱和,故不能析出,但NaHCO3的溶解度小,且溶液已达饱和,所以过多的NaHCO3以晶体形式析出.
探究一:用水作溶剂.在盛有5ml水和5ml汽油的两只试管中各加入1~2小粒高锰酸钾,可观察到的现象是高锰酸钾溶于水形成紫红色溶液,而高锰酸钾难溶于汽油,结论:同一种物质在不同溶剂中的溶解性不同.
探究二:用水区别物质.自选两种白色固体,用水区别它们,设计实验完成下表内容.
| 两种白色固体 | 主要操作、现象和结论 |
| 碳酸钙、氧化钙 | 分别将两种固体加水溶解,难溶于水的是碳酸钙,与水剧烈反应且有热量放出的是氧化钙 |
【查阅资料】?20℃时,五种物质的溶解度如下表.
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 | Na2CO3 |
| 溶解度/g | 36.0 | 21.0 | 37.2 | 9.6 | 21.5 |
【提出问题】20℃时,将11.7gNaCl和15.8gNH4HCO3同时放入盛有100g水的烧杯中,充分搅拌,静置,有晶体析出(温度仍为20℃).析出的晶体是什么?
【设计实验】设计方案,并进行实验.
(1)取少量晶体与熟石灰粉末混合、研磨,无明显现象.实验目的是证明晶体不是氯化铵.
(2)取少量晶体于试管中,加入盐酸,现象为有无色气体产生.
【实验结论】(3)析出的晶体是NaHCO3,晶体的质量为7.2g.
【实验拓展】(4)析出晶体的原因是NaCl和NH4HCO3溶于水未达饱和,所以不能以晶体析出,它们在水中解离出Na+、Cl-、NH4+、HCO3-,阴阳离子运动结合成NaHCO3和NH4Cl,由于NH4Cl溶解度较大,未达饱和,故不能析出,但NaHCO3的溶解度小,且溶液已达饱和,所以过多的NaHCO3以晶体形式析出.




 ”、“
”、“ ”、“
”、“ ”分别表示不同种元素的原子,下列四幅图中,可用来表示氧化物的是( )
”分别表示不同种元素的原子,下列四幅图中,可用来表示氧化物的是( )