题目内容
10.在锥形瓶甲中放入5g块状CaCO3,在锥形瓶乙中放5g CaCO3粉末,分别加入足量等质量分数的稀盐酸. 产生气体的质量与反应时间关系描述合理的是( )| A. |  | B. |  | C. |  | D. |  |
分析 由题目的信息可知:块状CaCO3和粉末状CaCO3都是5g,由质量守恒定律,加入足量的稀盐酸后,产生的二氧化碳气体一样多;但是粉末状的CaCO3与盐酸的接触面积大,进行分析解答.
解答 解:块状CaCO3和粉末状CaCO3都是5g,由质量守恒定律,加入足量的稀盐酸后,产生的二氧化碳气体一样多.
A、粉末状的CaCO3与盐酸的接触面积大,反应速率快;块状CaCO3接触面积小,反应速率慢;得到同样多的二氧化碳,甲用的时间长,乙用的时间短,本图象颠倒了,故选项错误.
B、块状CaCO3和粉末状CaCO3都是5g,加入足量的稀盐酸后,产生的二氧化碳气体一样多,故选项错误.
C、粉末状的CaCO3与盐酸的接触面积大,反应速率快;块状CaCO3接触面积小,反应速率慢;得到同样多的二氧化碳,甲用的时间长,乙用的时间短,故选项正确.
D、块状CaCO3和粉末状CaCO3都是5g,加入足量的稀盐酸后,产生的二氧化碳气体一样多,故选项错误.
故选:C.
点评 本题难度不大,明确产生的二氧化碳气体一样多、接触面积大的反应速率快是正确解答本题的关键.

练习册系列答案
相关题目
3.下列各组混合物共6.5克与足量盐酸反应,有可能生成0.18克氢气的是( )
| A. | 锌和镁 | B. | 铁和锌 | C. | 锌和铜 | D. | 铁和镁 |
1.在实验操作考查中,小明抽到的题目是“氧气的制取、收集和检验”.下图是他的主要实验步骤,其中操作有误的是( )
| A. |  点燃酒精灯 | B. |  收集气体 | C. |  检查装置气密性 | D. |  检验 |
18.硒是抗衰老元素,且能抑制癌细胞生长.“北大富硒康”中含有硒酸根离子(SeO42-)则在硒酸根离子中硒元素的化合价为( )
| A. | -2价 | B. | -4价 | C. | +4价 | D. | +6价 |
5.下列有关构成物质粒子的说法,正确的是( )
| A. | 分子一定比原子大 | |
| B. | 分子、原子都是化学变化中的最小粒子 | |
| C. | 物质状态发生变化,是因为粒子大小发生变化 | |
| D. | 分子、原子都是构成物质的粒子 |
15.钛(Ti)和钛合金被认为是21世纪的重要金属材料.已知某种钛原子核内有22个质子,其相对原子质量约为48.下列有关该原子的叙述正确的是( )
| A. | 核内有22个中子 | B. | 质量为48 | C. | 核外有22个电子 | D. | 核电荷数为26 |
2.下列的化学反应既不是化合反应,也不是分解反应的是( )
| A. | 水 $\stackrel{通电}{→}$氢气+氧气 | B. | 一氧化碳+氧气$\stackrel{点燃}{→}$ 二氧化碳 | ||
| C. | 铝+氧气$\stackrel{点燃}{→}$ 氧化铝 | D. | 乙炔+氧气$\stackrel{点燃}{→}$ 二氧化碳+水 |
19.如图表示的是化学基本反应类型的微观模型,(反应条件不出现)下列反应中与图中的反应类型一致的是( )
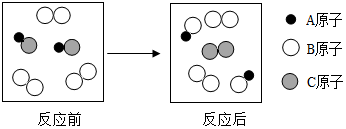

| A. | 2KClO3=2KCl+3O2↑ | B. | 2HI+Cl2=2HCl+I2 | ||
| C. | CO2+C=2CO | D. | HCl+NaOH=NaCl+H2O |
20.下面是关于物质分割的描述,其中分割到分子的是( )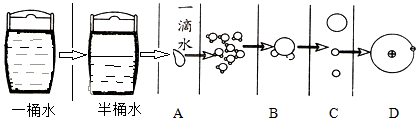

| A. | A | B. | B | C. | C | D. | D |