题目内容
20.如图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物.
(1)B装置玻璃管里可观察到的现象是红棕色粉末逐渐变黑.
(2)A装置中足量的氢氧化钠溶液作用是除净混合气体中的二氧化碳,反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;实验结束后,小红向A装置中滴加无色酚酞,发现溶液由无色变成红色,由此她确定装置A中溶质是氢氧化钠和碳酸钠,你同意她的观点吗不同意(填写“同意”或“不同意”),并说明理由碳酸钠的水溶液也能使无色酚酞变红.
(3)为了避免环境污染,还需要加尾气处理装置,可以加酒精灯点燃尾气.
(4)工业上可利用“铝热反应”焊接钢轨、冶炼难熔金属等,其原理是在高温下用铝将某些金属从其氧化物中置换出来.若用铝与四氧化三铁反应来制取25.2kg铁,理论上需要消耗铝的质量是多少?
分析 (1)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,进行分析解答;
(2)根据氢氧化钠的化学性质、碳酸钠溶液显碱性来分析;
(3)根据处理尾气的正确方法来分析;
(4)根据化学方程式和题中的数据进行计算.
解答 解:(1)用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,硬质玻璃管中变化的现象红棕色粉末逐渐变黑.故填:红棕色粉末逐渐变黑;
(2)氢氧化钠不与一氧化碳反应,但是可以与二氧化碳反应,所以A装置中足量的氢氧化钠溶液作用除净混合气体中的二氧化碳,二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠溶液也显碱性,能使无色的酚酞试液变红色,所以实验结束后,小红向A装置中滴加无色酚酞,发现溶液由无色变成红色,不能确定装置A中溶质是氢氧化钠和碳酸钠,故填:除净混合气体中的二氧化碳;CO2+2NaOH=Na2CO3+H2O;不同意;碳酸钠的水溶液也能使无色酚酞变红(其他合理答案都可);
(3)尾气中含有有毒的一氧化碳气体,一氧化碳具有可燃性,可以用酒精灯将其点燃处理;故填:酒精灯点燃尾气(其他合理答案都可);
(4)解:设需要消耗铝的质量为x
8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe
216 504
x 25.2kg
$\frac{216}{504}=\frac{x}{25.2kg}$
x=10.8kg
答:理论上需要消耗铝的质量是10.8kg.
点评 本题难度不大,掌握一氧化碳还原氧化铁的实验原理、现象等并能灵活运用是正确解答本题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | O2→H2O | B. | CuO→CO2 | C. | Fe(OH)3→FeCl3 | D. | CaCO3→Ca(OH)2 |
| A、化学常识 | B、化学与健康 |
| ①活性炭除异味是利用它的吸附性 ②合金、塑料、橡胶都属于合成材料 | ③人体缺乏碘易患甲状腺肿大 ④海鲜防腐可用甲醛溶液浸泡 |
| C、化学与生活 | D、化学与环境 |
| ⑤用汽油清洗油污属于乳化作用 ⑥燃烧法区分棉纤维和羊毛纤维 | ⑦使用无磷洗衣粉可减少水污染 ⑧使用乙醇汽油可减少空气污染 |
| A. | A | B. | B | C. | C | D. | D |
| A. | X气体排放到空气中,会造成空气污染 | |
| B. | 硫元素的化合价在化学反应前后没有发生改变 | |
| C. | 硫酸中硫元素与氧元素的质量比为1:2 | |
| D. | 该反应说明了碳具有还原性,浓硫酸具有氧化性 |
| A. | 电灯发光 | B. | 轮胎爆炸 | C. | 玻璃破碎 | D. | 葡萄酿酒 |
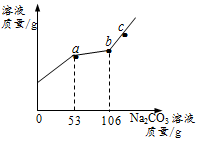 烧杯中有CaCl2与稀HCl的混合溶液50g,向烧杯中逐渐加入10.0% Na2CO3溶液,所得溶液的质量与所滴加Na2CO3溶液质量关系如图(不考虑生成气体在溶液中的溶解和其他物质的挥发).下列说法正确的是( )
烧杯中有CaCl2与稀HCl的混合溶液50g,向烧杯中逐渐加入10.0% Na2CO3溶液,所得溶液的质量与所滴加Na2CO3溶液质量关系如图(不考虑生成气体在溶液中的溶解和其他物质的挥发).下列说法正确的是( )| A. | a-b段产生气体 | |
| B. | c点溶液的pH>7 | |
| C. | b点时烧杯中物质的总质量为148.8g | |
| D. | a到b过程中,溶液中NaCl的质量分数在不断增大 |


 向l33.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示.求:
向l33.4克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如图所示.求: