题目内容
20.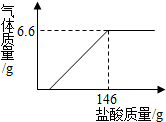 现将19.9g含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入一定溶质质量分数的盐酸,生成气体的质量与加入盐酸的质量关系如图所示.请计算
现将19.9g含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入一定溶质质量分数的盐酸,生成气体的质量与加入盐酸的质量关系如图所示.请计算(1)固体中碳酸钠的质量;
(2)恰好完全反应时溶液中氯化钠的质量;
(3)欲将恰好完全反应时所得溶液配制成20%的溶液需蒸发水的质量.
分析 根据固体的成分可知,发生的化学反应为盐酸与氢氧化钠、盐酸与碳酸钠反应,但只有硫、盐酸与碳酸钠反应生成二氧化碳气体,利用图象可知完全反应生成6.6g气体,然后代入化学反应方程式计算碳酸钠的质量,生成氯化钠的质量,最后计算溶质的质量分数.
解答 解:根据图示可知:完全反应生成6.6g二氧化碳气体
设碳酸钠质量为x,碳酸钠完全反应生成氯化钠的质量为y
(1)Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 117 44
x y 6.6g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{6.6g}$
x=15.9g
y=17.55 g
(2)设氢氧化钠完全反应生成氯化钠的质量为z
NaOH+HCl═NaCl+H2O
40 58.5
19.9g-15.9g z
$\frac{40g}{19.9g-15.9g}=\frac{58.5g}{z}$
z=5.85g
所以恰好完全反应时溶液中氯化钠的质量为:17.55g+5.85g=23.4g
(3)恰好完全反应时所得溶液质量为:19.9g+100g+146g-6.6g=259.3g
设蒸发水的质量为m
(259.3g-m)×20%=23.4g
m=142.3g
答案:
(1)固体中碳酸钠的质量为15.9g
(2)恰好完全反应时溶液中氯化钠的质量为23.4g
(3)需蒸发水的质量为142.3g
点评 本题较复杂,计算的知识点多,学生利用图象分析出二氧化碳的质量代入化学反应方程式计算是解答的突破口.

练习册系列答案
相关题目
11.下列叙述中,错误的是( )
| A. | 分子、原子、离子都是构成物质的基本粒子 | |
| B. | 不同元素的原子的核电荷数一定不同 | |
| C. | 在置换反应中,元素的化合价一定发生改变 | |
| D. | 核外电子排布相同的粒子一定属于同种元素 |
8.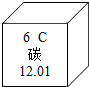 如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
 如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
如图是元素周期表中碳元素的相关信息,下列说法错误的是( )| A. | 碳的相对原子质量为12.01 | |
| B. | 碳元素位于元素周期表的第二周期 | |
| C. | 碳元素是形成化合物种类最多的元素 | |
| D. | 含有碳元素的物质都具有可燃性 |
15. 下列化学反应属于右边关系图中阴影部分的是( )
下列化学反应属于右边关系图中阴影部分的是( )
 下列化学反应属于右边关系图中阴影部分的是( )
下列化学反应属于右边关系图中阴影部分的是( )| A. | CuO+CO$\frac{\underline{\;高温\;}}{\;}$ Cu+CO2 | B. | 2H2O $\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑ | ||
| C. | CaO+H2O=Ca(OH)2 | D. | NH4Cl+NaOH=NaCl+NH3↑+H2O |
12.下列各种不同的“水”中,属于纯净物的是( )
| A. | 蒸馏水 | B. | 柠檬水 | C. | 糖水 | D. | 盐汽水 |
9.两种金属混合物30g,投入足量盐酸中,产生1g氢气,则组成该混合物的不可能是( )
| A. | Fe、Zn | B. | Al、Zn | C. | Mg、Al | D. | Mg、Cu |

