题目内容
9.两种金属混合物30g,投入足量盐酸中,产生1g氢气,则组成该混合物的不可能是( )| A. | Fe、Zn | B. | Al、Zn | C. | Mg、Al | D. | Mg、Cu |
分析 根据铁、锌、铝、镁会与酸反应生成氢气,铜不会与酸反应,然后才有极值法和均衡法进行计算.
解答 解:假设30克全部是纯金属,计算生成的氢气质量,
Fe-H2,Zn-H2,2Al-3H2,Mg-H2,
56 2 65 2 54 6 24 2
30g 1.1g 30g 0.92g 30g 3.3g 30g 2.5g
铜不会与酸生成氢气,通过分析可知,镁、铝混合物生成的氢气大于1g,故选C.
点评 本题主要考查混合物的计算,难度不大,注意利用平均值法解答比较简单.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
19.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如下表所示.下列说法中不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
| A. | 生成甲、丁两种物质的质量比为1:4 | |
| B. | 丙一定是该反应的催化剂 | |
| C. | 该反应为分解反应 | |
| D. | 乙、丁两种物质间反应的质量比为7:5 |
17. 如图是元素周期表中的硫元素及其原子结构示意图,下列说法正确的是( )
如图是元素周期表中的硫元素及其原子结构示意图,下列说法正确的是( )
 如图是元素周期表中的硫元素及其原子结构示意图,下列说法正确的是( )
如图是元素周期表中的硫元素及其原子结构示意图,下列说法正确的是( )| A. | 硫元素属于金属元素 | B. | 硫原子在化学反应中容易失去电子 | ||
| C. | 硫的相对原子质量为32.06g | D. | 硫离子最外层上有8个电子 |
14.下列化学式书写规范的是( )
| A. | 氧化镁mgO | B. | 硫酸铜cuSO4 | C. | 五氧化二氮N2O5 | D. | 氦气HE |
19.下列关于水的说法正确的是( )
| A. | 所有物质都易溶于水 | |
| B. | 可将工业废水任意排入内河 | |
| C. | 生活中常用肥皂水检验软水和硬水 | |
| D. | 水电解过程与电源正极连接的一端产生氢气 |
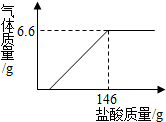 现将19.9g含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入一定溶质质量分数的盐酸,生成气体的质量与加入盐酸的质量关系如图所示.请计算
现将19.9g含氢氧化钠的碳酸钠固体中加入100g水充分溶解,向该溶液中逐滴加入一定溶质质量分数的盐酸,生成气体的质量与加入盐酸的质量关系如图所示.请计算 根据图中所示的实验请回答下列问题:
根据图中所示的实验请回答下列问题: