题目内容
11.如图为实验室制取气体的常用装置.
(1)仪器①的名称是长颈漏斗.
(2)以A 为发生装置,用高锰酸钾制取的氧气化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该装置中有一处错误是试管口没有放棉花团,收集一瓶较干燥的气体应用F.
(3)B、C 都可以作为制取二氧化碳发生装置,B装置相对C装置的优点是可以控制反应的开始与停止.
(4)酸的种类、浓度、固体的颗粒大小等因素会影响反应速率.为研究实验室制取二氧化碳的适宜条件,进行了如下五组实验:
药品 编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 大理石(mg) | 块状 | 块状 | 粉末状 | 粉末状 | 块状 |
| 盐酸(ng) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 | 稀硫酸 |
②实验甲与乙 (填编号)对照,是为了研究酸的浓度对反应速率的影响;
③实验戊与甲(填编号)对照,是为了研究酸的种类对反应速率的影响.
分析 (1)熟记仪器的名称;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气,为了防止高锰酸钾进入导管,通常在试管口塞一团棉花,根据收集氧气的方法来分析;
(3)根据装置的特点来分析;
(4))正确书写实验室制取二氧化碳反应的化学方程式;根据表格中信息,进行分析推测.
解答 解:(1)仪器①是长颈漏斗;故填:长颈漏斗;
(2)实验室用高锰酸钾制取氧气的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,因为反应不需要加热,发生装置应该选用A,为了防止高锰酸钾进入导管,试管口应放一团棉花,向上排空气法收集的氧气比较干燥;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口没有放棉花团;F;
(3)与C装置相比,B装置可以控制反应的开始与停止;故填:可以控制反应的开始与停止;
(4)①实验室制取二氧化碳是用大理石和稀盐酸反应,大理石的主要成分是碳酸钙,与盐酸反应生成氯化钙、水和二氧化碳,其化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②甲与乙对比,相同质量的块状大理石分别与稀盐酸与浓盐酸反应,根据产生气泡的速率推断出酸的浓度对反应速率的影响;故填:乙;
③实验戊与甲对照,相同质量的块状大理石分别与稀盐酸和稀硫酸反应,根据产生气泡的速率推断出酸的种类对反应速率的影响;故填:甲.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 硫酸钠 NaSO4 盐 | B. | 氧化钙 CaO 氧化物 | ||
| C. | 烧碱 KOH 碱 | D. | 甲烷 CH4 无机物 |
| A. | 滤纸上只有Ag | |
| B. | 滤渣中加入稀盐酸有气泡产生 | |
| C. | 滤纸上有Zn、Cu、Ag,滤液呈蓝色 | |
| D. | 滤纸上有Cu、Ag,滤液中有Zn2+、Cu2+ |
| 元素 | O | Mg | Al | Cl |
| 原子结构 示意图 |  | 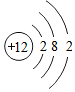 | 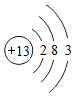 | 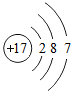 |
(2)氯原子在化学反应中易得到(填“得到”或“失去”)电子;带有1个单位负电荷,成为阴离子.
(3)从上图中可以知道Al3+与氧原子具有相同的电子层数.
| A. | 氧气 碳酸钙 空气 | B. | 氢气 硫酸钠 水 | ||
| C. | 生铁 食盐 冰水 | D. | 金刚石 熟石灰 石油 |
| A. | KCl(K2CO3)加足量稀盐酸、过滤、蒸发、结晶 | |
| B. | MnO2 (KCl)加水溶解、过滤、蒸发、结晶 | |
| C. | CuO(Cu)加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | BaSO4(BaCO3)加足量稀盐酸、过滤、洗涤、干燥 |
| A. | Cu>R>Mg | B. | Mg>R>Cu | C. | R>Mg>Cu | D. | Mg>Cu>R |
| A. | 吸入的气体比呼出的气体氧气含量大 | |
| B. | 吸入的气体比呼出的气体二氧化碳含量大 | |
| C. | 吸入的气体比呼出的气体水蒸气含量大 | |
| D. | 吸入的气体和呼出的气体氮气含量几乎没有变化 |