题目内容
19. 小红同学用如图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).
小红同学用如图总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).I.为了验证反应①,小红将无色酚酞试液滴入NaOH溶液中,溶液由无色变成红色.
II.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:CO2+2NaOH=Na2CO3+H2O.
III.为了验证反应③能够发生,你选择的物质是C.
A.Na2CO3 B.HCl C.FeCl3 D.Ba(NO3)2.
分析 Ⅰ.根据无色酚酞试液遇碱变成红色分析;
Ⅱ.根据氢氧化钠变质是因为氢氧化钠与空气中的二氧化碳反应分析;
III.根据复分解反应的条件:必须有水、沉淀或气体生成.
解答 解:Ⅰ.无色酚酞试液遇碱变成红色,所以无色酚酞试液滴入NaOH溶液中,溶液由无色变成红色,故填:红色;
Ⅱ.氢氧化钠变质是因为氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;故填:CO2+2NaOH=Na2CO3+H2O;
III.氢氧化钠与盐反应属于复分解反应,复分解反应的条件:必须有水、沉淀或气体生成.
A.Na2CO3和氢氧化钠不反应,故错误;
B.HCl是酸,不符合题意,故错误;
C.FeCl3和NaOH反应生成氢氧化铁沉淀,满足复分解反应的条件,故正确;
D.Ba(NO3)2和氢氧化钠不能满足复分解反应的条件,所以不反应,故错误;
故选C.
点评 在解此类题时,首先分析图示所表示的反应的实质,然后结合学过的知识和复分解反应的条件进行解.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
9.北大富硒康中的硒是人体所必需的微量元素之一,具有抗癌,保护心肌等需要功能.缺硒时,机体免疫功能降低,容易发生癌症和其他疾病.硒在元素周期表中的信息如图,有关硒的说法不正确的是( )


| A. | 硒原子的质子数为34 | B. | 硒原子的核外电子数为34 | ||
| C. | 硒原子的中子数为46 | D. | 硒原子的核电荷数为46 |
7.铬(Cr)为不锈钢主要的添加元素,含量一般在12%以上.铬的表面生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:
(1)铁生锈的主要条件是铁与空气中的氧气和水直接接触.
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
上述三种金属的活动性由强到弱的顺序是Mg、Cr、Cu.
(1)铁生锈的主要条件是铁与空气中的氧气和水直接接触.
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
11.有甲乙丙丁四种金属,只有甲在自然界主要以单质形态存在,四种金属中甲和丙不和稀盐酸反应,乙的盐溶液可以用金属丁所制的容器盛放,这种金属的活动性由强到弱的顺序( )
| A. | 乙>丁>丙>甲 | B. | 丙>丁>乙>甲 | C. | 甲>乙>丁>丙 | D. | 丙>乙>丁>甲 |
8.2007年诺贝尔化学奖授予德国化学家GerhardErtl,以表彰他在表面化学领域研究所取得的开拓性成就.某反应在Pt/Al2O3/Ba催化剂表面吸附与解吸作用的机理如图所示(图中HC表示碳氢化合物,nitrate指硝酸盐),该机理研究是指( )
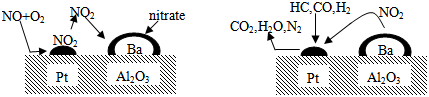

| A. | 催化剂参与反应活性研究 | B. | 金属变质机理 | ||
| C. | 汽车尾气催化转化处理 | D. | 氮气催化氧化机理 |


