题目内容
11.小明欲配制50g质量分数为5%的氢氧化钠溶液.如图是实验操作示意图.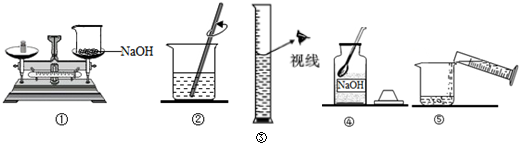
(1)计算需要氢氧化钠的质量为2.5g.需要水的体积为47.5mL.
(2)用上述图示的序号表示配制溶液的操作顺序:④①③⑤②;
(3)量取所需要的水应选择50ml(选填“10mL”“50mL”或“100mL”)量筒
(4)①的错误操作导致所配置的溶液的溶质质量分数偏小(选填“偏大”、“偏小”或“不变”),若其他操作均正确.①操作导致最后实际所配置的溶液的溶质质量分数为3%.
(5)③的错误操作导致所配置的溶液的质量分数偏小(选填“偏大”、“偏小”或“不变”),改正:视线与凹液面的最低处保持水平.
(6)配制好的氢氧化钠溶液要密封保存,其原因是易与二氧化碳反应而变质.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数求出溶质的质量,再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量,并据m=ρv计算水的体积.
(2)根据配制溶质质量分数一定的溶液的基本步骤进行分析解答.
(3)根据所量取水的体积确定所用量筒的量程.
(4)根据托盘天平的使用要遵循“左物右码”的原则进行分析解答.
(5)根据量筒读数时视线要与凹液面的最低处保持水平进行分析解答.
(6)根据氢氧化钠易与二氧化碳反应进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,50g质量分数为5%的氢氧化钠溶液,需氢氧化钠的质量=50g×5%=2.5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=50g-2.5g=47.5g,水的密度为1g/cm3,则根据V=$\frac{m}{p}$=$\frac{47.5g}{1g/cm3}$=47.5mL;
(2)配制50g质量分数为5%的氢氧化钠溶液的步骤:计算、称量(量取)、溶解、装瓶贴签,用图示的序号表示为:④①③⑤②;
(3)量取所需要的水应选50mL的量筒,减小误差;
(4)托盘天平的使用要遵循“左物右码”的原则,图①中氢氧化钠与砝码的位置颠倒,会导致称量的固体减小,则溶质的质量分数偏小;
①操作导致最后实际所配置的溶液的溶质质量分数$\frac{2g-0.5g}{50g}$×100%=3%;
(5)量取液体时,视线与液体的凹液面最低处保持水平,图中仰视刻度,导致量取的水偏大,使所配溶液溶质的质量分数偏小;
(6)配制好的氢氧化钠溶液要密封保存,因为氢氧化钠易与空气中的二氧化碳反应生成碳酸钠而变质;
故答案为:(1)2.5; 47.5;
(2)④①③⑤②;
(3)50ml;
(4)偏小;3%;
(5)偏小; 视线与凹液面的最低处保持水平;
(6)易与二氧化碳反应而变质
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、仪器的正确使用、氢氧化钠溶液的性质等是正确解答本题的关键.

 通城学典默写能手系列答案
通城学典默写能手系列答案| A. | 太阳能电池给路灯供电 | B. | 植物进行光合作用 | ||
| C. | 太阳能热水器把水烧热 | D. | 以上三项都不是 |
 化学变化多姿多彩,美丽如画,图中甲乙丙丁分别是CuO、C、CO、盐酸中的某一种,甲乙丙均能与丁发生化学反应,则丁是( )
化学变化多姿多彩,美丽如画,图中甲乙丙丁分别是CuO、C、CO、盐酸中的某一种,甲乙丙均能与丁发生化学反应,则丁是( )| A. | C | B. | CuO | C. | CO | D. | 盐酸 |
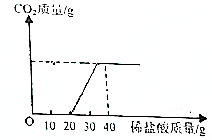 某造纸厂排放的废水中含有Na2CO3和NaOH,为测定废水中Na2CO3的质量分数,取50g废水样品于烧杯中,将40g稀盐酸分成4等份分4次慢慢加入到烧杯中,获得的实验现象和数据如表所示:
某造纸厂排放的废水中含有Na2CO3和NaOH,为测定废水中Na2CO3的质量分数,取50g废水样品于烧杯中,将40g稀盐酸分成4等份分4次慢慢加入到烧杯中,获得的实验现象和数据如表所示:| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸的质量(g) | 10 | 10 | 10 | 10 |
| 生成气体质量(g) | 0 | x | 1.2 | 1.0 |
(1)表中x的值为0;
(2)第2次加入稀盐酸充分反应后,溶液中的溶质是Na2CO3和NaCl(填化学式);
(3)反应产生CO2的质量为2.2g;
(4)计算该废水中Na2CO3的质量分数.
| 选项 | 待区分的物质 | 鉴别方法 |
| A | 合成纤维和纯羊毛 | 取样,分别灼烧,并闻气味 |
| B | CaCl2溶液和NaCl溶液 | 取样,分别加入肥皂水,观察泡沫是否丰富 |
| C | 稀盐酸和稀硫酸 | 取样,分别滴加石蕊试液,观察是否变红 |
| D | 碳粉和氧化铜 | 取样,分别加入足量稀硫酸,观察是否能溶解 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 食物腐败 | B. | 冰雪融化 | C. | 酒精挥发 | D. | 干冰升华 |