题目内容
1.如图1是元素周期表的一部分,据此回答下列问题.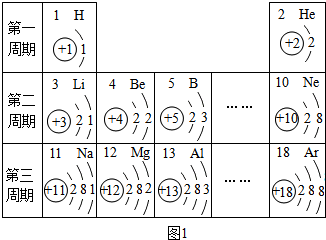
(1)表中12号元素的名称是镁,该元素的原子在化学反应中易失去(填“得到”或“失去”)电子,形成子离子符号是Mg2+
(2)原子序数为11和16的两种元素组成的化合物是Na2S (写化学式)
(3)图2是元素锶(Sr)的原子结构示意图,则x=38,锶元素的氧化物的化学式为SrO.通过图1表分析可知,锶元素位于元素周期表第五周期.
(4)图3中与锶元素化学性质相似的是A(填字母).

分析 (1)根据原子序数=核电荷数=质子数,由元素周期表中原子结构示意图的核内质子数进行分析解答;若最外层电子数≥4,则一般为非金属元素,在化学反应中易得电子,若最外层电子数<4,则一般为金属元素,在化学反应中易失去电子.
(2)原子序数是11的元素是钠元素,原子序数是16的元素是硫元素,据此进行分析解答.
(3)根据元素周期表中周期数等于原子核外电子层数进行分析解答;
(4)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切进行解答.
解答 解:(1)根据原子序数=核电荷数=质子数,表中12号元素的原子结构示意图中,核内质子数为12,其元素的名称为镁元素;该元素的原子最外层电子数为2,在化学反应中易失去2个电子,形成阳离子.
故填:镁:失;Mg2+
(2)钠元素常显+1价,硫元素显-2价,故填:Na2S
(3)元素周期表中周期数等于原子核外电子层数,由元素锶(Sr)的原子结构示意图,质子数等于核外电子数,所以x=2+8+18+8+2=38;锶原子的最外层电子数为2,容易失去2个电子,所以化合价为+2价,所以锶元素的氧化物的化学式为SrO;由元素锶(Sr)的原子结构示意图,其原子核外有5个电子层,锶元素位于元素周期表第五周期;
故填:38;SrO;五;
(4)元素的化学性质与最外层电子数有关,所以最外层电子数相同的元素化学性质相似,所以选择最外层电子数是2的元素即是,如镁元素等.
故填:A
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图的含义进行分析、解题的能力.

练习册系列答案
相关题目
11.下列现象的描述正确的是( )
| A. | 硫在氧气中燃烧,产生淡蓝色火焰 | |
| B. | 碳酸氢铵受热分解,生成白色固体 | |
| C. | 棉花和羊毛灼烧都产生烧焦羽毛的气味 | |
| D. | 铁与稀硫酸反应有气泡产生,溶液由无色变成浅绿色 |
12.下列对化学事实的解释错误的是( )
| A. | 花香四溢--分子在不断地运动 | |
| B. | CO有毒而CO2无毒--两种物质的分子构成不同 | |
| C. | 温度计中的水银热胀冷缩--原子的大小发生改变 | |
| D. | 水受热变成水蒸气--分子分裂成原子 |
9.如表是某指示剂在一定pH范围内所显示的颜色:
向滴有少量该指示剂的NaOH溶液中加入稀盐酸,有可能出现的颜色变化是( )
| 颜色 | 红 | 橙 | 绿 | 蓝 | 紫 |
| pH | 1~3 | 4~5 | 6~7 | 8~10 | 11~14 |
| A. | 由紫到绿 | B. | 由绿到蓝 | C. | 由橙到绿 | D. | 由红到紫 |
6.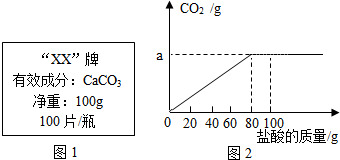 钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
(1)表中m的数值为25;n的数值为20.
(2)该品牌补钙药剂中CaCO3的质量分数是50%;图象中a的数值为8.8.
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)
 钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.(1)表中m的数值为25;n的数值为20.
(2)该品牌补钙药剂中CaCO3的质量分数是50%;图象中a的数值为8.8.
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)
| 第1次 | 第2次 | 第3次 | 第4次 | 第五次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | 30 | m | 20 | n |
13.实验操作是初中化学应掌握的基本技能之一,下列实验方案不合理的是( )
| A. | 加肥皂水区别硬水和软水 | B. | 用燃烧区别晴纶和羊毛纤维 | ||
| C. | 用水区别氢氧化钠和硝酸铵 | D. | 滴加石蕊溶液区别稀盐酸和雨水 |
10. 硅是一种半导体材料,可用于制作半导体器件和集成电路.还可以合金的形式使用.为了更好地了解硅元素,同学们查阅了元素周期表,下面从该图获取的信息中,不正确的是( )
硅是一种半导体材料,可用于制作半导体器件和集成电路.还可以合金的形式使用.为了更好地了解硅元素,同学们查阅了元素周期表,下面从该图获取的信息中,不正确的是( )
 硅是一种半导体材料,可用于制作半导体器件和集成电路.还可以合金的形式使用.为了更好地了解硅元素,同学们查阅了元素周期表,下面从该图获取的信息中,不正确的是( )
硅是一种半导体材料,可用于制作半导体器件和集成电路.还可以合金的形式使用.为了更好地了解硅元素,同学们查阅了元素周期表,下面从该图获取的信息中,不正确的是( )| A. | 硅元素的原子核内有14个质子 | B. | 硅元素属于非金属元素 | ||
| C. | 硅元素相对原子质量为28.09g | D. | 硅元素的原子核内有14个中子 |