题目内容
3.同学们用如图所示装置探究制取气体的原理、方法和性质.结合图1回答问题:
(1)写出指定仪器的名称:①锥形瓶,②长颈漏斗.
(2)用高锰酸钾制取氧气,应选择的发生装置是A(填序号);反应原理用化学方程式表示2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;为防止高锰酸钾粉末进入导管,应采用的措施是试管口放一团棉花;若使用E装置来收集氧气,实验结束时,应先从水槽中移除导管,再熄灭酒精灯,原因是防止水槽中的水倒吸炸裂试管.
(3)实验室中制取二氧化碳气体可选用的发生和收集装置是BC(填序号)
(4)利用如图2所示装置来验证二氧化碳气体的性质,要证明二氧化碳与氢氧化钠能够发生反应,加入试剂的顺序是先加入氢氧化钠溶液,后加入盐酸,气球的变化是气球先膨胀,后缩小.
分析 (1)依据常用仪器回答;
(2)依据高锰酸钾制取氧气的反应物状态、反应条件选择发生装置,并据氧气的密度、高锰酸钾制取氧气反应原理分析解答;
(3)依据制取二氧化碳的方法分析解答;
(4)氢氧化钠能和二氧化碳反应生成碳酸钠和水,碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳.
解答 解:
(1)标号仪器分别是锥形瓶和长颈漏斗;
(2)用高锰酸钾制取氧气时,需要加热,故选发生装置A;高锰酸钾加热生成锰酸钾、二氧化锰和氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;为防止高锰酸钾粉末进入导管,应采取的措施是在试管口放一团棉花;为防止水槽中的水倒吸炸裂试管,实验结束时,应先从水槽中移出导气管,再熄灭酒精灯.
(3)实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,故选发生装置B;二氧化碳的密度比空气大,易溶于水,故可用向上排空气收集;
(4)要证明二氧化碳气体与氢氧化钠能够发生反应,加入试剂的顺序是先加入氢氧化钠溶液,后加入盐酸,气球的变化是气球先膨胀,后缩小.
答案:
(1)①锥形瓶;②长颈漏斗
(2)A 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口放一团棉花 防止水槽中的水倒吸炸裂试管
(3)BC
(4)先加入氢氧化钠溶液,后加入盐酸;气球先膨胀,后缩小.
点评 掌握实验室制取氧气、二氧化碳、氢气的方法,及装置选取方法,才能顺利解答该题.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
14.化学基本概念是学好化学的基础.对下列有关概念的认识正确的是( )
| A. | 原子是最小的微粒,不可再分 | |
| B. | 塑料、合成纤维和合成橡胶属于合成材料 | |
| C. | 均一、稳定的液体一定是溶液 | |
| D. | 中和反应是指能够生成盐和水的反应 |
11.下列相关事实用微观粒子的知识解释不正确的是( )
| 选项 | 事实 | 解释 |
| A | 酒精溶液是混合物 | 由不同种分子构成 |
| B | 水结冰后体积变大 | 水分子体积变大 |
| C | 墙内开花墙外可嗅到花香 | 分子不断运动 |
| D | 氢氧化钠溶液能导电 | 溶液中存在自由移动的Na+和OH- |
| A. | A | B. | B | C. | C | D. | D |
15.除去下列各组物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |
12.对比实验是化学中常用的实验手段.下列探究不需要进行对比实验的是( )
| A. | 物质溶解性的大小 | B. | 可燃物燃烧的条件 | ||
| C. | 烧碱样品中氢氧化钠的含量 | D. | 影响金属与酸反应速率的因素 |
13.下列物质的名称、俗名、化学式对应正确的是( )
| A. | 乙醇 酒精 C2H5OH | B. | 氧气 臭氧 O3 | ||
| C. | 氢氧化钠 烧碱 Na2CO3 | D. | 氢氧化钙 生石灰 Ca(OH)2 |

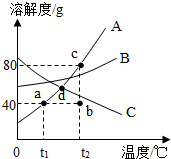 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答: