题目内容
12.对比实验是化学中常用的实验手段.下列探究不需要进行对比实验的是( )| A. | 物质溶解性的大小 | B. | 可燃物燃烧的条件 | ||
| C. | 烧碱样品中氢氧化钠的含量 | D. | 影响金属与酸反应速率的因素 |
分析 利用控制变量法的思想根据对比实验是指只允许一种变量,其它条件相同的实验结合具体实验的原理进行解答.
解答 解:A.比较不同物质的溶解性需要控制溶剂的种类、质量、温度等因素比较溶质溶解的最大限度,所以需要对比实验,故A错误;
B、铜片上的白磷与铜片上的红磷属于对照实验,都与氧气接触,都属于可燃物,变量是着火点不同,白磷着火点低,红磷着火点高,热水能达到白磷的着火点,达不到红磷的着火点,从而证明可燃物燃烧温度必须达到可燃物的着火点,所以需要对比实验,故B错误;
C、烧碱样品中氢氧化钠的含量只需要测定生成二氧化碳的多少,即可计算,不需要对比实验,故C正确;
D、影响金属与酸反应速率的因素有温度、浓度、反应物的接触面积,所以需要对比实验,故D错误.
故选:C.
点评 解答本题关键是要熟悉对比实验的设计思路,能够分析出变量和不变量,了解通过对比实验能验证出什么结论.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
2.下列示意图所示原子,最有可能属于金属元素原子的是( )
| A. | 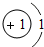 | B. | 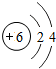 | C. | 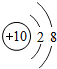 | D. | 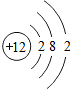 |
7.厨房中物质加入适量水后不能形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 植物油 | D. | 纯碱 |
4.新型材料的出现是材料发展史的重大突破.下列应用的材料属于复合材料的是( )
| A. |  玻璃钢茶几 | B. |  人面鱼纹彩陶盆 | C. |  金刚石薄膜 | D. |  银制器皿 |
1.某活动小组用未知金属X和Y分别进行了两个实验,实验结果如下:(实验中所有金属局面已打磨,且形状、大小以及稀盐酸的溶质质量分数均相同)
(1)Fe、X、Y三种金属的活动性由强到弱的顺序是Fe>Y>X;
(2)取两支试管分别放入铁和金属Y,同时加入等量的稀盐酸,预期可以观察到的现象是铁和Y的表面有气泡生成,铁的表面产生的气泡快;将金属Y加入到X的硝酸盐溶液中,预期可以观察到的现象是在Y的表面有红色物质生成;
(3)现有X、Y两种金属粉末的混合物,设计实验将X和Y充分分离,写出实验操作步骤.(提示:分离混合物需加入稍过量的试剂以达到最大限度的分离)
| 实验操作 | 金属X | 金属Y |
| 分别将金属放入稀盐酸中 | 没有变化 | 有气泡生成 |
| 分别将铁片插入金属X、Y的硝酸盐溶液中 | 铁片表面附着红色固体 | 铁片表面附着银白色固体 |
(2)取两支试管分别放入铁和金属Y,同时加入等量的稀盐酸,预期可以观察到的现象是铁和Y的表面有气泡生成,铁的表面产生的气泡快;将金属Y加入到X的硝酸盐溶液中,预期可以观察到的现象是在Y的表面有红色物质生成;
(3)现有X、Y两种金属粉末的混合物,设计实验将X和Y充分分离,写出实验操作步骤.(提示:分离混合物需加入稍过量的试剂以达到最大限度的分离)

 二氧化碳不仅能产生温室效应,还能作化工原料.
二氧化碳不仅能产生温室效应,还能作化工原料.




