题目内容
11.鉴别物质的方法错误的是( )| A. | 用燃着的木条鉴别空气和二氧化碳 | B. | 用水鉴别生石灰和石灰石 | ||
| C. | 用酚酞鉴别食盐水和稀醋酸 | D. | 用氯化钡溶液鉴别稀盐酸和稀硫酸 |
分析 鉴别题,当给出待鉴别物质以及拟采用的试剂和方法时,可以直接从拟采用的试剂和方法推测对应的实验原理,从而分析待鉴别物质是否对应明显的现象差别.
A、二氧化碳不能支持燃烧,空气中含有氧气,能支持燃烧;
B、氧化钙溶于水,并和水反应放热,碳酸钙不溶于水;
C、酚酞试液遇到碱性溶液变成红色;
D、硫酸和氯化钡会产生沉淀.
解答 解:A、燃烧的木条鉴别气体,是利用气体是否助燃的,氧气支持燃烧,而二氧化碳不支持燃烧.当燃着的木条插入集气瓶后,木条燃烧无明显变化的原气体为空气,而木条熄灭的原气体为二氧化碳.可以鉴别;
B、生石灰和水反应放热,而碳酸钙不溶于水,也没有明显的温度变化,可以鉴别;
C、食盐水为中性溶液,稀醋酸为酸性溶液,都不能使酚酞试液变色,不能鉴别;
D、氯化钡和稀硫酸混合会产生白色沉淀,而和稀盐酸没有明显现象,可以鉴别;
故选项为:C.
点评 在鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,然后根据性质的不同,选择适当的试剂,根据出现不同的现象才能鉴别.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
1.金属用途广泛,其结构和性质等是化学的重要研究内容.
(1)如图1是铝的原子结构示意图.

①下列说法不正确的是C.
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
②铝作为地壳中含量最丰富的金属,却直到19世纪末才被人类广泛应用于生活,这主要是跟铝的化学性质比较活泼有关,铝制品之所以耐腐蚀,是由于4Al+3O2═2Al2O3(用化学方程式表示).
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了图2实验,并对溶液A和固体B的成分进行了分析和实验探究.
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2 ②Zn (NO3)2、AgNO3
③Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是②(填标号),其理由是银的活动性比铜弱,若铜被置换出来,溶液中一定没有硝酸银;
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整.
(3)图3是工业炼铁示意图.工业炼铁的设备是炼铁高炉,其中,焦炭的作用是燃烧提供能量和做还原剂;有铁生成的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,炼得的铁是混合物(填“纯净物”或“混合物”).
(1)如图1是铝的原子结构示意图.

①下列说法不正确的是C.
A.铝原子的质子数为13
B.在化合物中铝通常显+3价
C.铝是地壳中含量最多的元素
D.铝可作导线是由于它具有良好的导电性
②铝作为地壳中含量最丰富的金属,却直到19世纪末才被人类广泛应用于生活,这主要是跟铝的化学性质比较活泼有关,铝制品之所以耐腐蚀,是由于4Al+3O2═2Al2O3(用化学方程式表示).
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了图2实验,并对溶液A和固体B的成分进行了分析和实验探究.
【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2 ②Zn (NO3)2、AgNO3
③Zn (NO3)2、Cu(NO3)2
④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是②(填标号),其理由是银的活动性比铜弱,若铜被置换出来,溶液中一定没有硝酸银;
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整.
| 实验步骤 | 现 象 | 有关反应的化学方程式 | 结论 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | Zn+2HCl═ZnCl2+H2↑ | 固体B中所含金属有 Zn、Cu、Ag |
19. 染发剂中含一种着色剂叫对苯二胺,其结构如图,关于对苯二胺的说法正确的是( )
染发剂中含一种着色剂叫对苯二胺,其结构如图,关于对苯二胺的说法正确的是( )
 染发剂中含一种着色剂叫对苯二胺,其结构如图,关于对苯二胺的说法正确的是( )
染发剂中含一种着色剂叫对苯二胺,其结构如图,关于对苯二胺的说法正确的是( )| A. | 对苯二胺由碳、氢、氮原子构成 | |
| B. | 对苯二胺中相对分子质量158g | |
| C. | 对二苯胺中碳元素的质量分数最大 | |
| D. | 对苯二胺中碳元素和氢元素的质量比为3:4 |
6.下列变化中,属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 钢铁生锈 | C. | 工业制氧气 | D. | 车胎爆炸 |
19. 实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
(1)反应生成氢气的质量为0.4g(结果精确到0.1g,下同).
(2)计算参加反应的锌的质量,写出必要的计算过程.
 实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.
实验室利用金属锌与稀硫酸反应制取氢气,另一种物质为硫酸锌.实验的相关数据如下表.| 气体发生装置内物质的总质量 | |
| 反应前 | 50g |
| 充分反应后 | 49.6g |
(2)计算参加反应的锌的质量,写出必要的计算过程.

 钙的一种特殊氧化物W(CaxOy)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.某化学兴趣小组针对W的组成进行了实验,实验装置如图.
钙的一种特殊氧化物W(CaxOy)广泛应用于水产养殖、污水处理等领域,是优良的供养剂.某化学兴趣小组针对W的组成进行了实验,实验装置如图.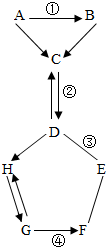 如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答:
如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、F都是单质,气体C常用于灭火,G是最轻的气体.请你回答: