题目内容
9.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为8g;
(3)所用稀盐酸中溶质的质量分数为多少.
分析 (1)由第四次实验数据可知,剩余的7.80g固体即为样品中铜的质量,铜的质量与样品质量比可计算出黄铜样品中铜的质量分数,而样品的质量=9.10g+0.65g=9.75g;
(2)根据加水稀释前后溶液中溶质质量不变,由40g7.3%的稀盐酸中溶质质量与浓盐酸的质量分数的比计算需要浓盐酸的质量;
(3)利用第二次实验所消耗锌的量,根据反应的化学方程式,计算出所加10g稀盐酸中溶质的质量,由溶质的质量分数公式,求出所用稀盐酸中溶质的质量分数;
解答 解:(1)由第二次实验可知,第一次加入10g稀盐酸时,反应消耗锌的质量为0.65g,则原黄铜样品的质量=9.10g+0.65g=9.75g;由第四次实验可知,样品中铜的质量7.80g
黄铜样品中铜的质量分数=$\frac{7.80g}{9.75g}$×100%=80%
故答案为:80%.
(2)需要浓盐酸的质量=$\frac{40g×7.3%}{36.5%}$=8g
故答案为:8g;
(3)设10g稀盐酸中HCl的质量为y
Zn+2HCl═ZnCl2+H2↑
65 73
0.65g y
$\frac{65}{0.65g}=\frac{73}{y}$
y=0.73g
所用稀盐酸中溶质的质量分数=$\frac{0.73g}{10g}$×100%=7.3%
故答案为:所用稀盐酸中溶质的质量分数为7.3%;
点评 分析每次加入10g稀盐酸固体剩余物质量的变化,可对反应进行的情况进行判断,这是解决本题的基础.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
19.决定元素种类的是原子的( )
| A. | 中子数 | B. | 电子数 | C. | 最外层电子数 | D. | 质子数 |
20. 如图“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是( )
如图“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是( )
 如图“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是( )
如图“→”表示一种金属能把另一种金属从其盐溶液中置换出来,则甲、乙、丙三种金属的活泼性由强到弱的顺序是( )| A. | 甲、乙、丙 | B. | 乙、丙、甲 | C. | 丙、甲、乙 | D. | 甲、丙、乙 |
5.为减少汽车尾气中铅的排放,提倡使用无铅汽油.无铅汽油一般是在汽油中加入甲基叔丁基醚,其化学式为CH3OC(CH3)3.关于甲基叔丁基醚叙述正确的是( )
| A. | 甲基叔丁基醚的相对分子质量为76 | |
| B. | 甲基叔丁基醚中碳、氢元素质量比为5:12 | |
| C. | 甲基叔丁基醚中碳元素的质量分数约为68.2% | |
| D. | 甲基叔丁基醚是由5个碳原子、12个氢原子和1个氧原子构成 |
10.下列图象分别与操作相对应,其中合理的是( )
| A. | 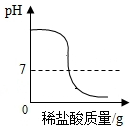 向一定量氢氧化钠溶液中滴加稀盐酸 | |
| B. | 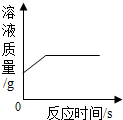 向一定量硝酸银溶液中加入一定量锌 | |
| C. | 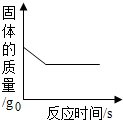 向一定量二氧化锰固体中加入一定量过氧化氢溶液 | |
| D. | 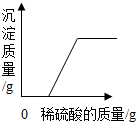 向一定量氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 |
