题目内容
10.下列图象分别与操作相对应,其中合理的是( )| A. | 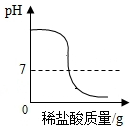 向一定量氢氧化钠溶液中滴加稀盐酸 | |
| B. | 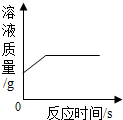 向一定量硝酸银溶液中加入一定量锌 | |
| C. | 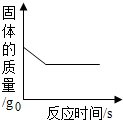 向一定量二氧化锰固体中加入一定量过氧化氢溶液 | |
| D. | 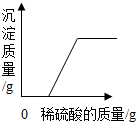 向一定量氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 |
分析 A.根据碱中加酸的原理来分析;
B.根据金属与盐的反应来分析;
C.根据催化剂的概念来分析;
D.根据氯化钡能与稀硫酸反应生成了硫酸钡沉淀来分析.
解答 解:A.氢氧化钠溶液pH大于7,滴加稀盐酸时溶液的pH逐渐减少,当稀盐酸过量时,溶液的pH小于7,故正确;
B.锌与硝酸银溶液发生置换反应生成银和硝酸锌,方程式为:Zn+2AgNO3=2Ag+Zn(NO3)2,
380 189
由此可见,反应后溶液的质量减少,故错误;
C.在过氧化氢分解的反应中,二氧化锰是催化剂,其质量在反应前后不变,故错误;
D.向一定量的氢氧化钠和氯化钡的混合溶液中滴加稀硫酸生成了硫酸钡沉淀,当氯化钡完全反应时生成的沉淀的质量不再增加,故错误.
故选A.
点评 本题通过坐标的形式考查了常见物质的性质,正确辨别坐标所表示的意义及坐标所表示的量的关系是解决问题的关键.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
9.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,洋洋同学取一定质量的黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
(1)黄铜样品中铜的质量分数为80%;
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为8g;
(3)所用稀盐酸中溶质的质量分数为多少.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.10 | 8.45 | 7.80 | 7.80 |
(2)用36.5%的浓盐酸配制40g上述稀盐酸,需要浓盐酸的质量为8g;
(3)所用稀盐酸中溶质的质量分数为多少.
1.下列物质的用途跟其化学性质相关的是( )
| A. | 干冰用于人工降雨 | B. | 氮气用于食品保存 | ||
| C. | 稀有气体用于制作霓虹灯 | D. | 铜用作电线 |
19.以下四组离子,能大量共存且能形成无色透明溶液的是( )
| A. | Fe3+Ag+ Cl- SO42- | B. | Mg2+Cu2+Cl- OH- | ||
| C. | H+ Na+ K+ NO3- | D. | H+ Ba2+NO3- SO42- |
20.下列四个图象能正确反映对应变化关系的是( )
| A. |  向一定量锌粒中加入过量稀硫酸 向一定量锌粒中加入过量稀硫酸 | |
| B. |  加热一定质量的氯酸钾和二氧化锰的混合物 加热一定质量的氯酸钾和二氧化锰的混合物 | |
| C. |  电解水 | |
| D. |  向一定量CaCl2溶液中加入Na2CO3溶液 向一定量CaCl2溶液中加入Na2CO3溶液 |
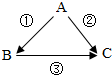 A、B、C为初中化学常见的物质,它们有如图所示转化关系(部分生成物已略去).
A、B、C为初中化学常见的物质,它们有如图所示转化关系(部分生成物已略去).