题目内容
5.氢气具有还原性,能在加热条件下与CuO发生反应:H2+CuO═Cu+H2O.某同学为了验证氢气还原氧化铜的产物,设计了如下由A、B、C三部分组成的实验装置.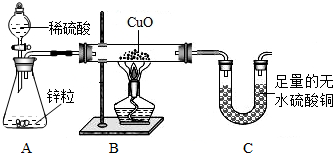
(1)实验中,用锌粒和稀硫酸反应制取氢气.实验开始前需要先检验氢气的纯度,然后应先通一段时间氢气,再加热氧化铜进行反应,其主要目的是排净试管中的空气,防止加热时发生爆炸;
(2)能确认反应生成水的实验现象是无水硫酸铜变蓝;
(3)上述实验装置还存在不足之处,为了达到实验目的,使根据现象得出的结论更严格更科学,请你提出修改意见:在AB之间放一个干燥装置.
分析 (1)根据氢气具有可燃性,点燃氢气与空气的混合物容易发生爆炸;
(2)白色的无水硫酸铜遇到水会变蓝色;
(3)制备的氢气中可能混有水蒸气.
解答 解:(1)氢气具有可燃性,点燃或加热氢气与空气的混合物容易发生爆炸,所以先通一段时间氢气,是赶尽装置中的空气,防止爆炸.故填:排净试管中的空气,防止加热时发生爆炸;
(2)白色的无水硫酸铜遇到水会变蓝色,故填:无水硫酸铜变蓝;
(3)制取的氢气中会混有水蒸气,为了防止对实验结果的干扰,应在AB之间防止一个干燥装置,故填:在AB之间放一个干燥装置.
点评 本题为典型的实验探究题,熟练掌握氢气还原氧化铜的性质和实验才能准确解答该题,要分析清楚每步实验的目的即可准确解答该题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列物质反应现象描述正确的是( )
| A. | 铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成黑色固体 | |
| B. | 硫在空气中燃烧发出微弱的淡蓝色火焰,放出大量的热,生成二氧化硫 | |
| C. | 磷在空气中燃烧放出大量的热,生成大量的烟雾 | |
| D. | 铝丝插入到硫酸铜溶液,有红色固体析出,溶液逐渐由蓝色变为浅绿色 |
16.在相同的条件下,碘难溶于水,易溶于汽油,说明影响碘的溶解能力的因素是( )
| A. | 温度 | B. | 压强 | C. | 溶质的性质 | D. | 溶剂的性质 |
13.下列几种常见饮料中,不含有机物的是( )
| A. |  | B. |  | C. |  | D. |  |
10.石灰石是某市主要矿产之一.学校研究生学习小组为了测定当地矿山石灰厂中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200克,平均分成4份,进行实验,结果如下:
(1)这种测定方法是定量(填定性或定量)测定.
(2)上表中m的数值是4.4.
(3)试计算这种石灰石矿中碳酸钙的质量分数.
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/克 | 5 | 10 | 15 | 20 |
| 生成CO2的质量/克 | 1.76 | 3.52 | 4.4 | m |
(2)上表中m的数值是4.4.
(3)试计算这种石灰石矿中碳酸钙的质量分数.
14.下列说法不正确的是( )
| A. | 目前,我国的空气质量指标分为优、良、轻度污染、中度污染和重度污染五级 | |
| B. | 酸雨是由于空气中过多的二氧化碳而造成的 | |
| C. | 保护空气要发展“绿色工业”,使用清洁能源,植树造林,绿化环境 | |
| D. | 森林能净化空气,被称为“地球之肺” |
15.下列是实验室常见的物质,其溶液两两混合,能产生蓝色沉淀的是( )
| A. | BaCl2、Na2SO4 | B. | NaOH、CuSO4 | C. | HCl、Ca(OH)2 | D. | H2SO4、K2CO3 |
 如图所示装置,O点是一固定点,活塞连接金属滑片(只滑动不旋转),活塞运动滑动变阻器阻值随之改变.试管内是空气和足量的白磷,烧杯中盛放足量生石灰.闭合电键小灯泡发光后再向烧杯中加入数滴含有酚酞试液的水,试推测:
如图所示装置,O点是一固定点,活塞连接金属滑片(只滑动不旋转),活塞运动滑动变阻器阻值随之改变.试管内是空气和足量的白磷,烧杯中盛放足量生石灰.闭合电键小灯泡发光后再向烧杯中加入数滴含有酚酞试液的水,试推测: