题目内容
某化学小组的同学进行了如图的实验,把固体乙洗涤后加入稀盐酸有气体放出.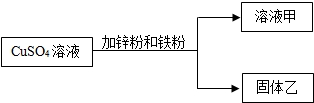
(1)固体乙的成分可能是什么?
(2)溶液甲中一定含有的溶质是 (写化学式)
(3)写出上述过程中可能发生反应的一个化学方程式 .

(1)固体乙的成分可能是什么?
(2)溶液甲中一定含有的溶质是
(3)写出上述过程中可能发生反应的一个化学方程式
考点:盐的化学性质,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据置换反应的特点和金属活动性规律分析作答;
(2)根据(1)的分析结论进一步分析作答;
(3)写出上述过程中可能发生反应的一个化学方程式即可.
(2)根据(1)的分析结论进一步分析作答;
(3)写出上述过程中可能发生反应的一个化学方程式即可.
解答:解:在CuSO4溶液中加入锌粉和铁粉,由于锌比铁的活动性强,锌先与硫酸铜发生置换反应生成硫酸锌和单质铜,若锌粉反应完以后硫酸铜有剩余,则铁粉与硫酸铜继续发生置换反应生成硫酸亚铁和单质铜.
(1)若锌粉反应完以后硫酸铜有剩余,把固体乙洗涤后加入稀盐酸有气体放出,说明其中一定含有铁粉;若锌粉与硫酸铜反应完以后有剩余,若把固体乙洗涤后加入稀盐酸有气体放出,固体乙的成分就是单质铜、铁和锌;故固体乙的成分可能是Cu、Fe或Cu、Fe、Zn;
(2)综上分析,溶液甲中一定含有的溶质是ZnSO4;
(3)上述过程中可能发生反应的一个化学方程式Zn+CuSO4═ZnSO4+Cu;
故答案为:
(1)Cu、Fe或Cu、Fe、Zn;
(2)ZnSO4;
(3)Zn+CuSO4═ZnSO4+Cu;
(1)若锌粉反应完以后硫酸铜有剩余,把固体乙洗涤后加入稀盐酸有气体放出,说明其中一定含有铁粉;若锌粉与硫酸铜反应完以后有剩余,若把固体乙洗涤后加入稀盐酸有气体放出,固体乙的成分就是单质铜、铁和锌;故固体乙的成分可能是Cu、Fe或Cu、Fe、Zn;
(2)综上分析,溶液甲中一定含有的溶质是ZnSO4;
(3)上述过程中可能发生反应的一个化学方程式Zn+CuSO4═ZnSO4+Cu;
故答案为:
(1)Cu、Fe或Cu、Fe、Zn;
(2)ZnSO4;
(3)Zn+CuSO4═ZnSO4+Cu;
点评:本题难度不大,掌握金属的化学性质并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
鉴别下列物质所使用的方法或试剂,错误的是( )
| A、氧气与氮气--闻气味 |
| B、氯化钠与碳酸钠--稀盐酸 |
| C、铝与铝合金--比较硬度 |
| D、氢氧化钠固体和碳酸钙固体--水 |
下列物质中,加水充分振荡后,pH最大的是( )
| A、CaO |
| B、NaCl |
| C、CO2 |
| D、Cu(OH)2 |