题目内容
4.同学们在学习碱的化学性质时,进行了如图所示的实验:
(1)乙实验中滴加氢氧化钠溶液后,可观察到的现象是瘪气球膨胀起来,发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O
(2)丙实验中观察到的实验现象是产生白色沉淀;
(3)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:指示剂、水、氯化钠、碳酸钙
②还含有能使废液呈碱性的物质,能使废液呈碱性的物质是什么?
同学们有如下猜想:
小丽认为:有氢氧化钠和碳酸钠; 小明认为:只有碳酸钠; 小平认为:只有氢氧化钙
你认为还可能是只有氢氧化钠(写一种猜想)
【实验设计】小芳想用氯化钙溶液来验证以上三个同学的猜想,通过查阅资料获悉氯化钙溶液呈中性,并设计如下实验,请你将小芳的实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | ①有白色沉淀,溶液呈红色 | 小丽的猜想正确 |
| ②有白色沉淀,溶液呈无色 | 小明的猜想正确 | |
| ③不产生沉淀,溶液呈红色 | 小平的猜想正确 |
分析 (1)氢氧化钠和二氧化碳反应生成碳酸钠和水;
(2)碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠;
(3)氢氧化钠溶液显碱性,能使酚酞试液变红色;
碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠.
解答 解:(1)乙实验中滴加氢氧化钠溶液后,氢氧化钠和二氧化碳反应生成碳酸钠和水,锥形瓶中气体压强减小,在外界大气压作用下,瘪气球膨胀起来,氢氧化钠和二氧化碳反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:瘪气球膨胀起来;2NaOH+CO2═Na2CO3+H2O.
(2)丙实验中碳酸钠和氢氧化钙反应生成白色沉淀碳酸钙和氢氧化钠,因此观察到产生白色沉淀.
故填:产生白色沉淀.
(3)同学们有如下猜想:
小丽认为:有氢氧化钠和碳酸钠; 小明认为:只有碳酸钠; 小平认为:只有氢氧化钙;还可能是只有氢氧化钠.
故填:只有氢氧化钠.
【实验设计】
实验过程如下表所示:
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置 | ①有白色沉淀,溶液呈红色 | 小丽的猜想正确 |
| ②有白色沉淀,溶液呈无色 | 小明的猜想正确 | |
| ③不产生沉淀,溶液呈红色 | 小平的猜想正确 |
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.下列物质中,既可与酸反应又可与水反应的是( )
| A. | CaO | B. | CO2 | C. | CaCO3 | D. | Na2SO4 |
15.有一瓶无色液体X,分成三等份,向其中分别加入少量的KCl溶液、Na2CO3溶液和Ba(NO3)2溶液,产生的现象如下表.则物质X是下列选项中的( )
| KCl溶液 | Na2CO3溶液 | Ba(NO3)2溶液 | |
| 物质X | 无明显现象 | 产生气体 | 产生白色沉淀 |
| A. | 澄清石灰水 | B. | 稀盐酸 | C. | 稀硫酸 | D. | 酚酞试液 |
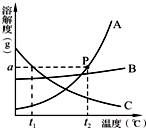 A、B、C三种物质的溶解度曲线如图所示.
A、B、C三种物质的溶解度曲线如图所示. 某学习小组对实验室久置的NaOH的变质程度进行探究.先称取13.3g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.
某学习小组对实验室久置的NaOH的变质程度进行探究.先称取13.3g 的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示. 某温度时一小试管内盛有的KNO3的饱和溶液,试管底部还存有少许KNO3固体,(温度越高KNO3的溶解能力越强)将小试管放入盛有水的烧杯内,向烧杯内的水中加入固体氢氧化钠,发现小试管内的固体物质逐渐溶解,根据所学知识解释小试管内固体物质逐渐溶解的原因是NaOH遇水放热,而KNO3的溶解度随温度升高而升高,从而导致未溶解的KNO3继续溶解.
某温度时一小试管内盛有的KNO3的饱和溶液,试管底部还存有少许KNO3固体,(温度越高KNO3的溶解能力越强)将小试管放入盛有水的烧杯内,向烧杯内的水中加入固体氢氧化钠,发现小试管内的固体物质逐渐溶解,根据所学知识解释小试管内固体物质逐渐溶解的原因是NaOH遇水放热,而KNO3的溶解度随温度升高而升高,从而导致未溶解的KNO3继续溶解. 如图,该装置有洗气、检验及储气等多种用途.
如图,该装置有洗气、检验及储气等多种用途.